《2026药品器械行业监管新趋势,企业合规准备指南》
各位药品、器械行业的伙伴们,2026年的监管大幕已经拉开,政策的风向正清晰指向"数字化合规"与"全链条追溯"。对于药品、医疗器械企业来说,过去靠纸质资料补漏洞、事后整改的模式早已行不通,以电子证据链为核心的合规体系,将成为企业生存与发展的必备能力。
作为深耕药品器械合规领域的证据链科技公司,我们第一时间拆解了今年监管政策的核心调整,帮你理清趋势、备好工具,从容应对新要求。
监管新趋势:从"结果合规"到"过程可追溯"
2026年药械监管的核心逻辑,已经从”检查资料是否符合要求”,转向"验证合规过程是否真实、可追溯",其中”电子证据链"和"数据可追溯性”是两大关键抓手:
电子证据链成为合规核心载体:
政策明确要求,临床试验、生产流程、营销推广等全环节的合规记录,需以不可篡改的电子证据形式留存,纸质资料仅作为补充
电子证据需具备"生成-留存-调用"全链路的可追溯性,任何操作痕迹都要留痕可查
数据追溯能力纳入监管考核:
监管部门将通过数字化系统,对企业合规数据进行穿透式核查
数据断点、证据链不完整将直接触发风险预警,成为现场检查的重点线索
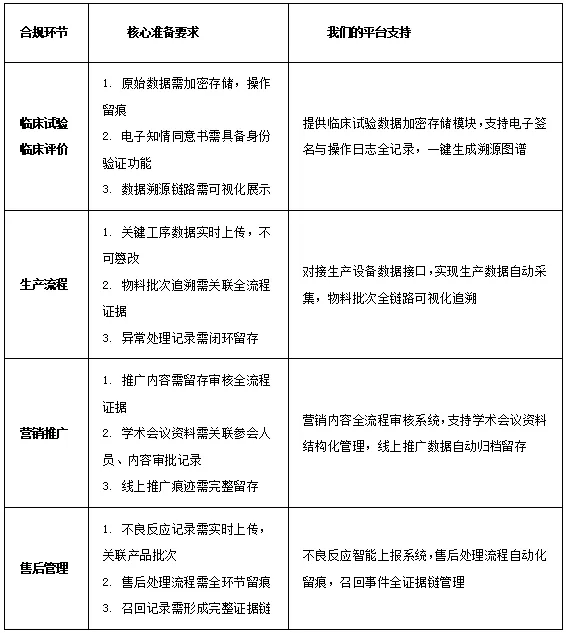
证据链数字化转型准备清单:提前布局,应对监管
结合政策要求和我们服务数百家企业的实操经验,整理出这份《证据链数字化转型准备清单》,帮你逐一排查风险,搭建符合新要求的合规体系:
我们如何帮企业构建合规证据链?
作为专注药械合规领域的科技公司,我们凭借"技术+专业"的双重优势,为企业提供从"合规咨询"到"系统落地"的全流程服务:
合规诊断与方案定制
·结合企业业务场景,开展合规风险排查,出具数字化转型专属方案
·匹配监管政策要求,帮企业梳理各环节证据链的核心节点与留存标准
电子证据链系统搭建
·提供全环节电子证据留存模块,支持数据加密、操作留痕、不可篡改
·打通各业务系统数据接口,实现合规数据自动采集、统一管理
合规运营与持续优化
·定期开展政策解读与系统培训,确保企业员工熟练掌握数字化合规工具
·实时跟进监管动态,为企业提供合规体系持续优化建议
前车之鉴:证据链缺失,成为违规重灾区
我们梳理了2025年药械行业的典型违规案例,发现80%以上的处罚,根源都在于证据链缺失或不完善:
某医疗器械企业因临床评价资料中,原始数据与报告结论无法溯源,被要求暂停产品注册,整改周期长达6个月
某药品生产企业因生产记录电子数据存在篡改痕迹,被处以货值金额3倍的罚款,直接经济损失超千万
某药企因学术推广资料缺乏审批留痕证据,被认定为"虚假宣传",企业信用评级降档,影响后续招标资格
这些案例都在提醒我们:证据链是合规的生命线,也是应对监管的核心底气。
2026年的药械监管,已经进入"数字化精准监管"的新阶段,企业的合规能力不再是"加分项",而是"准入门槛"。作为你的合规伙伴,我们将持续聚焦政策动态,以技术赋能药械企业的合规转型,帮你筑牢数字化合规护城河。
如果你的企业正面临证据链数字化转型的困惑,欢迎随时联系我们,获取免费的合规诊断服务,为你的企业定制专属转型方案。


