
[1] ZHANG Y, CHU M, SAMALA S, et al. Mobile genetic elements drive the evolution and multidrug resistance of Salmonella infantis along the United States poultry production line [J]. BMC Genomics, 2026, 27(1).
文献
原文标题:Mobile genetic elements drive the evolution and multidrug resistance of Salmonella infantis along the United States poultry production line
作者与单位:
第一作者:张玉洁
通讯作者:Vivian C.H. Wu
主要机构:美国农业部农业研究局,西部地区研究中心,农产品安全与微生物研究所 (Produce Safety and Microbiology Research Unit, U.S. Department of Agriculture, Agricultural Research Service, Western Regional Research Center, Albany, CA, USA)
发表信息: BMC Genomics , 2026 , DOI: 10.1186/s12864-026-12607-z
文章类型: 原创性研究论文
核心关键词:
婴儿沙门氏菌
全基因组测序
巨型质粒 pESI
可移动遗传元件
多重耐药性
摘要
原文摘要:BACKGROUND: Salmonella is the primary enteric pathogen related to foodborne illnesses worldwide, posing significant public health concerns. Amongst the diversity and pathogenicity of over 2000 Salmonella serovars, Salmonella Infantis (S. Infantis) ranks among the top Salmonella serovars implicated in foodborne outbreaks, with thousands of reported cases annually in the United States. Moreover, the incidence of S. Infantis infections has spread rapidly worldwide from the U.S. to Europe, where more than 50% of isolated S. Infantis strains have developed antibiotic resistance. Previous studies have demonstrated that antibiotic resistance genes (ARGs), particularly those carried by plasmids, contribute to the persistence and spread of multipledrug-resistant (MDR) Salmonella strains in various environments. However, the information regarding the multidrug resistance and spread of S. Infantis is scarce. Hence, the objectives of this study were to characterize antibiotic-resistant S. Infantis isolated from the poultry production line in the United States and to examine the correlation between mobile genetic elements and bacterial resistome evolution. RESULTS: A total of 9 S. Infantis strains were isolated from poultry production lines in 2022, including comminuted chicken, raw intact/nonintact chicken, and chicken carcass. These strains were further subject to antimicrobial susceptibility tests, whole-genome sequencing, and bioinformatic analysis. Most strains were MDR and phenotypically resistant to five or more antibiotics, such as Streptomycin and Tetracycline. The complete bacterial genome results showed that all isolates had a dsDNA chromosome with a GC content of 52.3% and an average genome size of 4,730 kb, belonging to the sequence type 32. The genomic characterization of S. Infantis isolates revealed that each strain contained one IncFIB mega-plasmid with lengths from 289 to 327 kb. Five or more ARGs were detected in each strain, most of which were located in the mega-plasmids and bordered by diverse mobile genetic elements, including transposons, integrons, and prophages. The common ARGs present in the mega-plasmids included bla(CTX-M-65), aac(3)-IV, tetA, suil1, dfrA14, ant(3'')-Ia and floR. Moreover, the majority of whole-genome sequencing (WGS)-derived ARG profiles had concordant phenotypic traits. CONCLUSION: These findings reveal the genomic features and antimicrobial resistance profiles of S. Infantis strains from poultry production lines in the United States, indicating the potential of mobile genetic elements-driven S. Infantis resistome development.
摘要重述:
背景: 婴儿沙门氏菌是全球食源性疾病爆发的首要血清型之一,其多重耐药菌株在全球迅速蔓延,但相关机制信息匮乏。
方法: 本研究从美国禽类生产线(鸡肉碎、整鸡、鸡胴体)分离了9株婴儿沙门氏菌,通过抗菌药物敏感性试验、全基因组测序和生物信息学分析进行研究。
结果: 多数菌株为多重耐药,对五种及以上抗生素耐药。基因组分析发现,所有菌株均属于ST32型,并携带一个289-327 kb的IncFIB巨型质粒。多数耐药基因位于此巨型质粒上,且两侧伴有转座子、整合子和前噬菌体等可移动遗传元件。基因型与耐药表型基本一致。
结论: 本研究揭示了美国禽类生产线上婴儿沙门氏菌的基因组特征和耐药谱,表明可移动遗传元件驱动了其耐药组的形成与发展。
引言/背景
研究领域: 食品安全微生物学与细菌耐药性流行病学。聚焦于人畜共患病原体沙门氏菌在食品供应链中的传播、进化及多重耐药性产生的分子机制。
知识缺口:
尽管婴儿沙门氏菌的多重耐药现象日益严重,尤其是其能获得并传播耐药基因的特性,但其耐药性形成和传播的具体分子机制,特别是可移动遗传元件的作用,相关信息仍然匮乏。
针对美国禽类生产环境中婴儿沙门氏菌的基因组特征与耐药性进化的关联性研究尚不充分。
本文目标: 本研究旨在表征从美国禽类生产线中分离的耐抗生素婴儿沙门氏菌的特性,并探究可移动遗传元件与细菌耐药性进化之间的相关性。
材料与方法
核心模型/材料: 2022年从美国各地(NY, GA, AR等)禽类生产线上分离的9株婴儿沙门氏菌,样本来源包括鸡肉碎、整鸡、非整鸡和鸡胴体。
关键技术:
核心基因组多位点序列分型:用于菌株聚类,构建系统发育树。
基因预测: 使用PHASTER预测前噬菌体,ABRicate和BacAnt预测耐药基因、可移动遗传元件和毒力因子。
耐药表型鉴定: 采用纸片扩散法,测试菌株对26种抗生素的敏感性。
全基因组测序: 使用Oxford Nanopore Technologies的MinION平台进行长读长测序,以获取完整的细菌基因组(包括染色体和质粒)。
生物信息学分析:
研究设计: 这是一项横断面观察性研究。对从常规食品安全检查中获得的9株分离株进行表型耐药测试和基因组测序,随后进行基因型-表型关联分析,并深入挖掘基因组中可移动遗传元件的构成。
简易示意图:菌株收集 → 药敏试验 (表型) → DNA提取 → 纳米孔长读长测序 → 基因组组装与注释 (基因型) → 比较基因组学与关联分析 (表型-基因型比对,鉴定ARGs、MGEs、毒力因子) → 结论。
数据分析: 主要使用cgMLSTFinder进行分型分析,iTOL构建系统发育树,PlasmidFinder鉴定质粒类型,并通过SPIFinder分析沙门氏菌毒力岛。各类软件均使用默认参数。
结果
Table 1 & Table 2 (耐药表型与基因组概览)
核心发现: 确认了9株来自不同州和鸡肉产品的婴儿沙门氏菌,均为ST32型。大部分菌株对5种及以上抗生素耐药,被定义为多重耐药菌株。
关键数据: 4株菌(4900, 5221, 9861, 9799)表现出最强MDR表型,分别对14、14、15、16种抗菌药物耐药。所有菌株基因组大小约4.73 Mb,GC含量52.3%。
逻辑关系: 此部分回答了“这些菌株是谁,有多耐药”的基本问题,为后续探究耐药性的遗传基础提供了明确的表型和基因组背景。
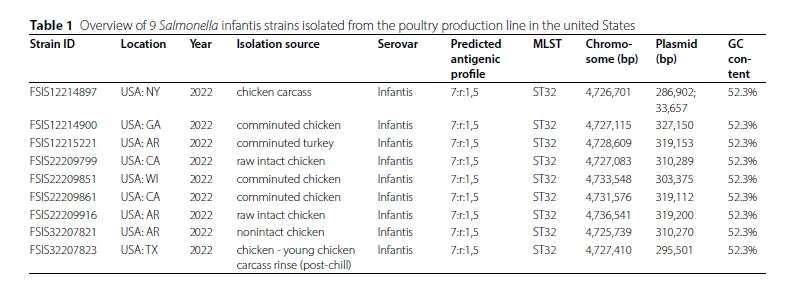
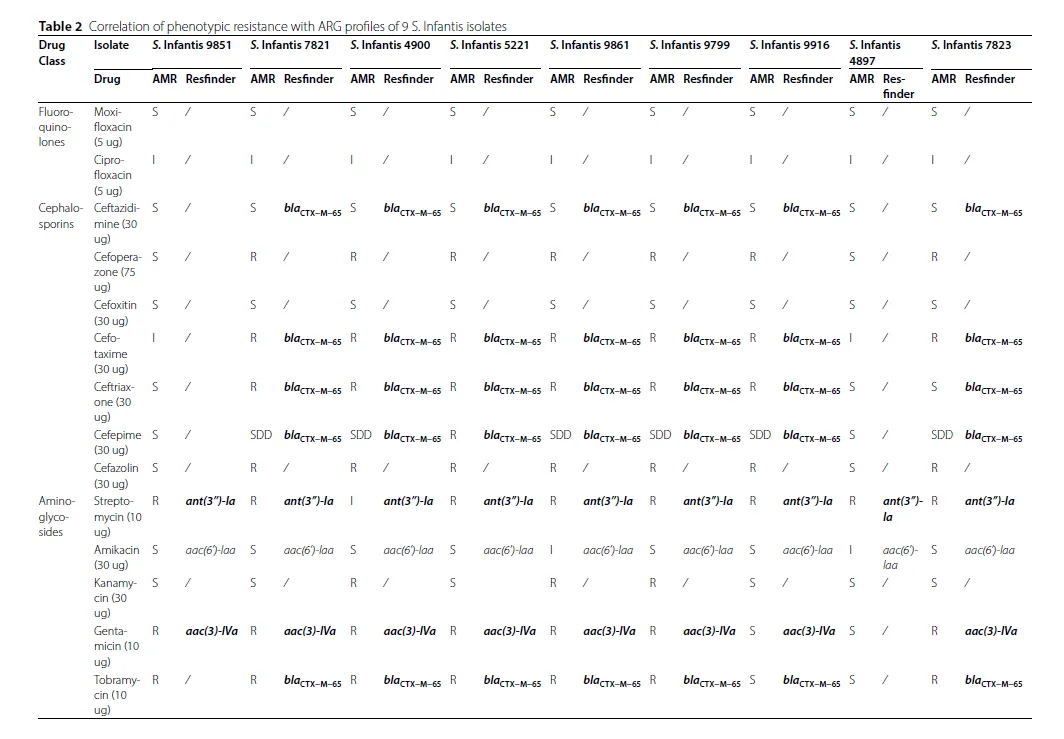
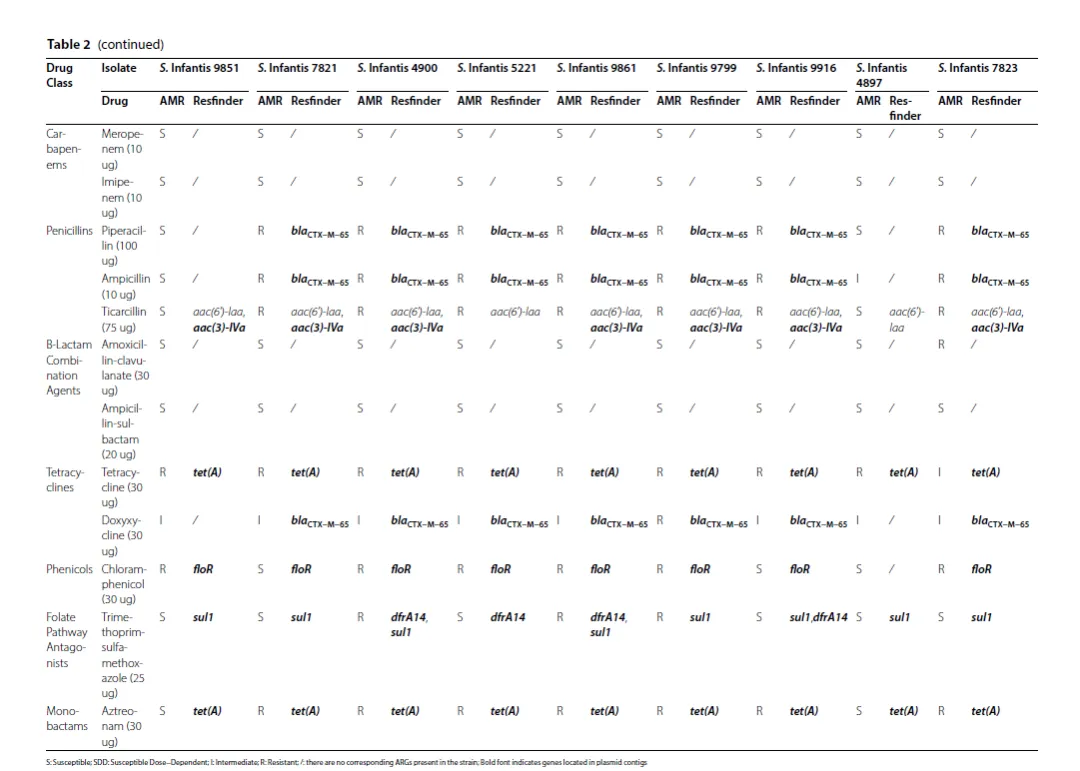
Fig. 1 (系统发育树与毒力岛)
核心发现: 基于核心基因组MLST,9株菌分为三个进化簇,但与地理来源无明显关联。每株菌携带约22个沙门氏菌毒力岛。
关键数据: 菌株4897单独成簇1;4900、7823、9799为簇2;其余5株为簇3。
逻辑关系: 此结果为故事设立了进化框架,表明美国禽类生产线上的婴儿沙门氏菌并非单一克隆,但其核心基因组高度相似。驱动它们分化的因素可能在于附属基因组,如质粒和可移动元件。

Fig. 2 & Table 2 (巨型质粒上的耐药基因与可移动元件结构)
核心发现: 每个菌株都携带一个类似pESI的IncFIB巨型质粒,这是多重耐药性的主要载体。质粒上的耐药基因被整合子、转座子等MGEs包围,形成了不同的耐药基因簇结构。
关键数据: 常见ARGs包括
blaCTX-M-65、aac(3)-IV、tetA、sul1、dfrA14、ant(3")-Ia和floR。例如,在菌株9916、5221、9861中,blaCTX-M-65基因侧翼是转座子Tn602。菌株4900的巨型质粒上,一个完整的前噬菌体内部包含了6个ARGs,其中两个dfrA14基因分别位于两个In2-14整合子中。所有巨型质粒都携带一个含有ant(3")-Ia和sul1基因的In498类整合子。逻辑关系: 这是全文的核心结果,直接验证了引言中的假说。它清晰地展示了“可移动遗传元件驱动耐药性”这一抽象概念的物理结构:ARGs被整合子和转座子捕获,镶嵌在巨型质粒上,甚至被前噬菌体携带,从而在不同菌株间形成多样的耐药谱。
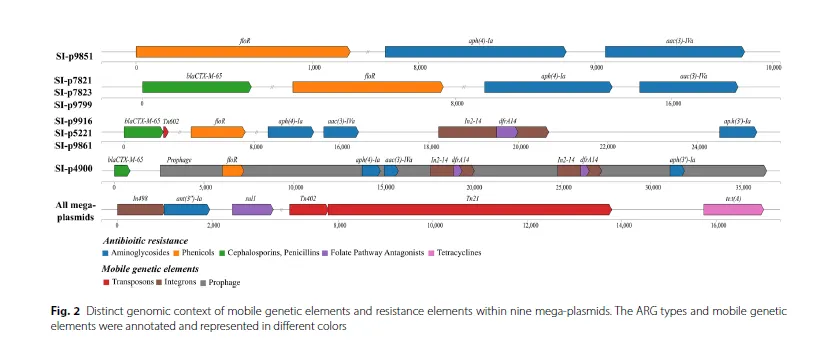
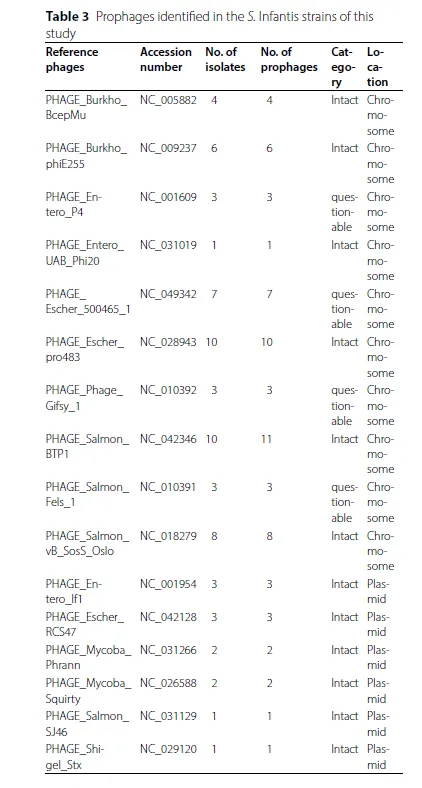
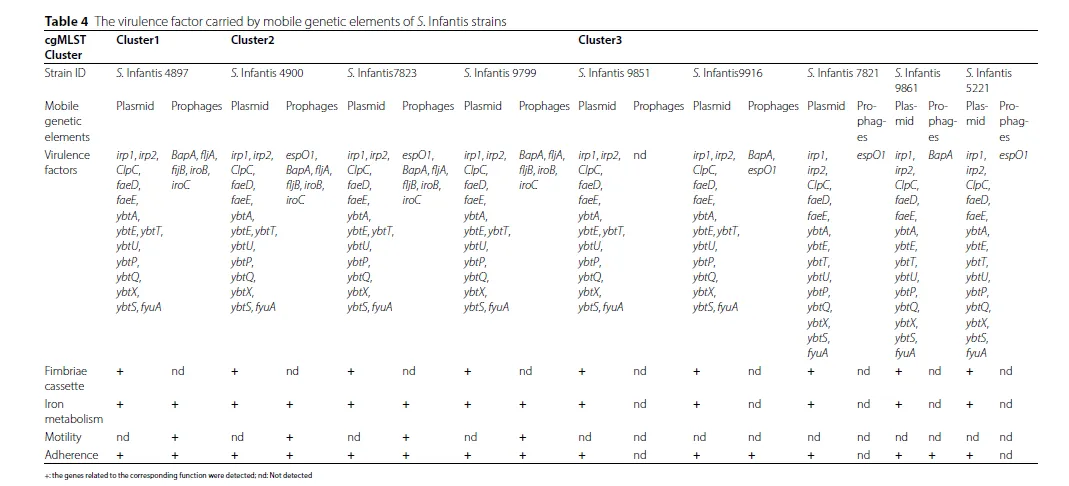
Table 3 & Table 4 (前噬菌体与毒力因子)
核心发现: 染色体和前噬菌体本身也携带毒力因子,且其分布与进化簇相关。尤其是前噬菌体中的毒力基因,可能影响不同进化簇菌株的致病潜力。
关键数据: 簇1和簇2菌株的前噬菌体普遍携带与黏附、运动和代谢相关的毒力基因(如
BapA,fljA,iroB),而簇3菌株的前噬菌体几乎不携带这些基因。巨型质粒本身携带一套保守的毒力因子,如耶尔森菌强毒力岛相关的铁载体合成基因簇。逻辑关系: 在揭示了MGEs介导的耐药性进化后,这部分结果进一步表明MGEs(如前噬菌体)也参与了菌株毒力的分化。这表明pESI质粒和前噬菌体共同塑造了细菌的适应性和致病潜力,使耐药和毒力的进化交织在一起。
讨论与结论
核心结论重申: 美国禽类生产线上的抗生素耐药婴儿沙门氏菌,其多重耐药表型主要由一个类似pESI的巨型质粒所介导。质粒上的耐药基因被多种可移动遗传元件包围,这一结构是驱动耐药组演化的关键。
机制阐释: 作者提出,转座子(如Tn602, Tn402, Tn21)和整合子(如In2-14, In498)等MGEs,通过捕获、重排和传播耐药基因,使得pESI质粒上的耐药基因含量在不同菌株间产生高度可变性,从而形成了多样的多重耐药谱。例如,整合子In2-14携带的dfrA14基因盒和Tn602相邻的blaCTX-M-65基因。
与既有研究的对话:
一致性: 本研究证实了ST32是婴儿沙门氏菌的一个全球流行序列型。发现的常见耐药基因组合(如
blaCTX-M-65,tetA,floR)在全球多地的婴儿沙门氏菌中均有报道。创新/矛盾: 本文首次在pESI质粒的前噬菌体基因组内部发现了成簇的耐药基因(菌株4900),这为ARGs的水平转移提供了一个新的、更为“嵌套”的传播载体视角。尽管全球流行,但核心基因组聚类与地理来源无相关性,这与其他研究一致,再次强调了是质粒等移动元件在驱动其全球传播中的关键作用。
研究的局限性与坦诚:
基因型与表型的矛盾未解释: 文中提到,尽管检测到了
sul1和dfrA14基因,但菌株未表现出对叶酸通路拮抗剂的耐药性;对头孢哌酮和头孢唑林的耐药性也无法用鉴定出的ARGs合理解释。作者尚未对这些矛盾现象给出解释。相关性未证明因果: 研究揭示了MGEs与ARGs的物理关联,但并未通过实验(如接合转移实验)直接证明这些MGEs介导了ARGs的转移。
未来展望与意义:
理论意义: 深化了对婴儿沙门氏菌“移动耐药组”进化的理解,揭示了质粒、转座子、整合子、前噬菌体等多层次MGEs协同驱动耐药性的模型。
实践意义/应用前景: 研究结果强调了监控禽类产品中携带pESI质粒的婴儿沙门氏菌的重要性。靶向pESI质粒或关键的MGEs,可能成为控制MDR婴儿沙门氏菌传播的新策略。
作者建议的下一步研究:
通过测定最低抑菌浓度,进一步研究耐药基因谱与表型耐药之间的精准关联。
深入研究pESI质粒上携带耐药基因的前噬菌体,在介导耐药性传播和促进菌株进化中的作用。
探究pESI质粒上单个遗传单元(如ARGs、金属耐受模块、毒力因子)的调控机制及其与宿主(禽类和哺乳动物)的相互作用。
个人笔记
研究亮点:
技术优势: 使用纳米孔长读长测序技术,获得了完整的闭合基因组,这对于解析由重复序列组成的复杂MGEs结构(尤其是巨型质粒)至关重要,是短读长测序无法比拟的。
结构可视化: Fig. 2 直观地展示了巨型质粒上耐药基因和MGEs的线性排列,堪称“耐药岛”的建筑蓝图,将抽象的“可移动元件驱动耐药”概念具象化。
发现的新意: 发现前噬菌体作为“套娃”结构的外壳,包裹并保护内部的多个ARGs和整合子,这是对耐药基因传播载体认知的拓展。
存疑之处:
存在基因型(如
sul1)与表型(对磺胺类敏感)不符的情况,作者未深入探讨,可能是因为相关基因失活突变、表达水平低或存在未知的抗性机制,这一点值得商榷。样本量仅为9株,尽管分析深入,但代表性有限,发现的三个进化簇及其毒力/耐药特征能否代表美国禽类生产线的整体情况仍需更大规模研究证实。
对你的启发:
研究范式: 证明了在耐药性研究中,“表型-基因型-MGE结构”三位一体的分析模式非常强大,是未来研究可借鉴的范本。
关注焦点转移: 提示我们在追踪MDR病原体时,不能仅停留在鉴定耐药基因,更要关注其上游的“移动平台”(如pESI)和“移动模块”(如整合子、转座子),这才是进化与传播的根源。
一句话概括:
本论文通过全基因组测序与精细的比较基因组学分析,揭示了美国禽类生产线上的多重耐药婴儿沙门氏菌,其耐药性进化是由一个类似pESI的巨型质粒所驱动,该质粒作为一个“移动耐药岛”,通过整合子、转座子乃至前噬菌体等多层次可移动遗传元件,不断捕获和重排耐药基因,从而塑造了菌株多样化的多重耐药谱。

