
▲3月19-20日 第十一届成都生物医药创新者峰会
扫码报名
声明:因水平有限,错误不可避免,或有些信息非最及时,欢迎留言指出。本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及);本文不构成任何投资建议。
药融圈监测显示:NEOK Bio是一家专注于双特异性抗体偶联药物(双抗ADC)研发的新药企业,其总部位于美国加利福尼亚州,成立于2025年,由全球抗体工程领域的领军韩国企业ABL Bio孵化而来,其战略目标是研发新一代抗体偶联药物,以解决实体瘤治疗中尚未被满足的临床需求,助力突破传统ADC药物在耐药性等方面的局限。
关联阅读:
礼来制药,投资一家亚洲Biotech(双抗ADC)
该公司的核心股东为ABL Bio,联合礼来基金(Lilly Asia Ventures)主导了其7500万美元的A轮融资,所筹资金全部用于推进核心双抗ADC候选药物的临床研发工作。
NEOK Bio的布局核心围绕创新双抗ADC技术平台展开,依托双抗原靶向设计,相较于传统单特异性ADC药物,大幅提升了ADC疗法的疗效与安全性,致力于为具有高临床价值的实体瘤适应症打造差异化的药物研发管线,践行双抗ADC“1+1>2”的协同治疗理念。
公司由拥有20余年肿瘤药物研发及商业化经验的生物技术行业资深人士Mayank Gandhi担任首席执行官(CEO),组建了顶尖的研发团队,其中包括具备丰富ADC偶联化学经验的首席科学官(CSO)Jon Tsuji(Seagen早期核心科学家)。
在产品线进展方面,NEOK Bio目前拥有两款核心双抗ADC药物:NEOK001(研发代码前身为ABL206)是一款同类首创的靶向B7-H3/ROR1的双抗ADC,采用拓扑异构酶I抑制剂作为载荷,于2026年1月获得美国食品药品监督管理局(FDA)的研究性新药(IND)批准;计划于2026年上半年启动I期临床试验,初步临床数据预计于2027年发布。
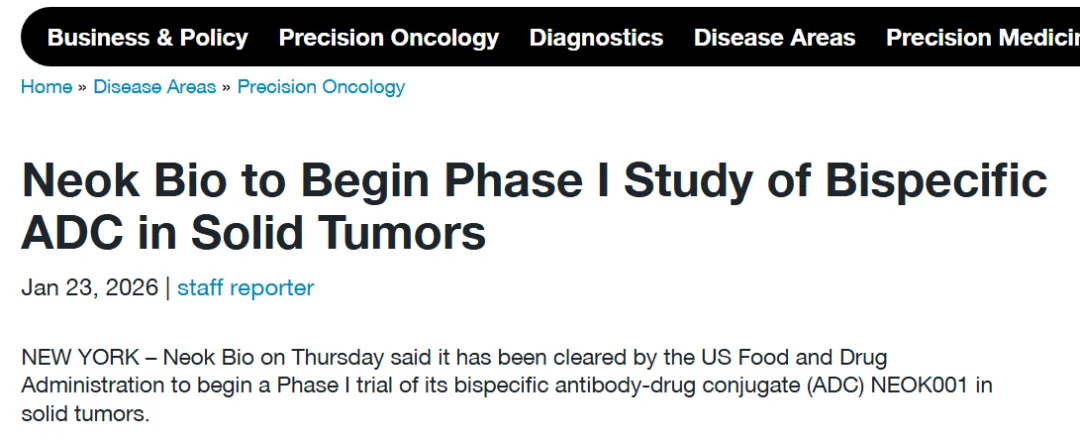
NEOK002(前身为ABL209)是一款靶向EGFR/MUC1的实体瘤适应症双抗ADC,公司计划于2026年第一季度提交IND申请并启动临床研究。作为NEOK Bio首个进入临床研发阶段的候选药物,NEOK001在临床前实体瘤模型中已展现出优异的体内疗效,标志着该公司在新一代双抗ADC研发领域迈出了重要一步,也奠定了其作为美国创新ADC领域新兴领军企业的地位。
参考资料:
药融圈数据;
摩熵医药pharma.bcpmdata.com(原药融云数据);
FDA/EMA/PMDA;
KBR(https://www.koreabiomed.com);
https://pulse.mk.co.kr/news/english/11285602;
https://www.marketscreener.com/news/abl-bio-neok-bio-submit-u-s-ind-for-phase-1-clinical-trial-of-abl209-n-ce7e5bd2d98af325;
https://www.businesswire.com/news/home/20260121856133/en/NEOK-Bio-Receives-FDA-IND-Approval-for-NEOK001-A-First-In-Class-B7-H3ROR1-Bispecific-ADC-for-Treatment-of-Solid-Tumor-Cancers;

活动推荐
创新无界,蓉城有约 | 药融圈NDC·成都生物医药创新者峰会


活动推荐
创新无界,蓉城有约 | 药融圈NDC·成都生物医药创新者峰会



