医药革命:AI制药企业B轮融资创纪录,远超传统大模型
相信对于关注AI制药的小伙伴,肯定也关注到了Isomorphic Labs近期21亿美元的B轮融资,是全球 AI 制药单轮融资历史最高,接近 OpenAI(2023 年 10 月,23 亿美元)、Anthropic(2024 年,20 亿美元)的单轮规模,远超绝大多数通用大模型融资。要知道这仅仅是一家成立5年,尚无任何药物进入临床,也无营收的创业公司,其核心技术关键是AlphaFold(诺奖技术)+IsoDDE 引擎,被誉为AI 药物发现的 “基础设施” 级平台。恰好2026年2月10日,Isomorphic Labs发布了一篇博客《The Isomorphic Labs Drug Design Engine unlocks a new frontier beyond AlphaFold》,详细介绍了IsoDDE引擎,我觉得核心关键词是“泛化”,生物与化学空间仍有大量未知领域待探索,模型必须具备超越训练数据集、泛化预测全新未知生物系统的能力。而IsoDDE展现了这样的能力。我把原文链接放在了文末,以下是原文翻译,供大家参考。
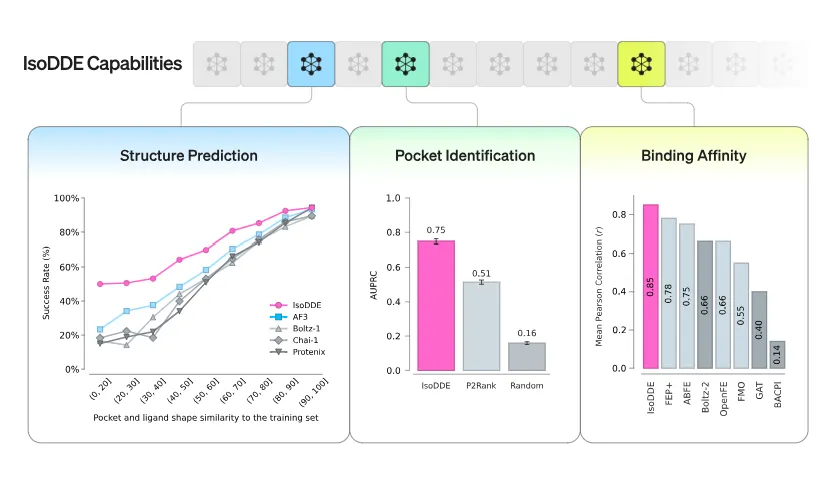
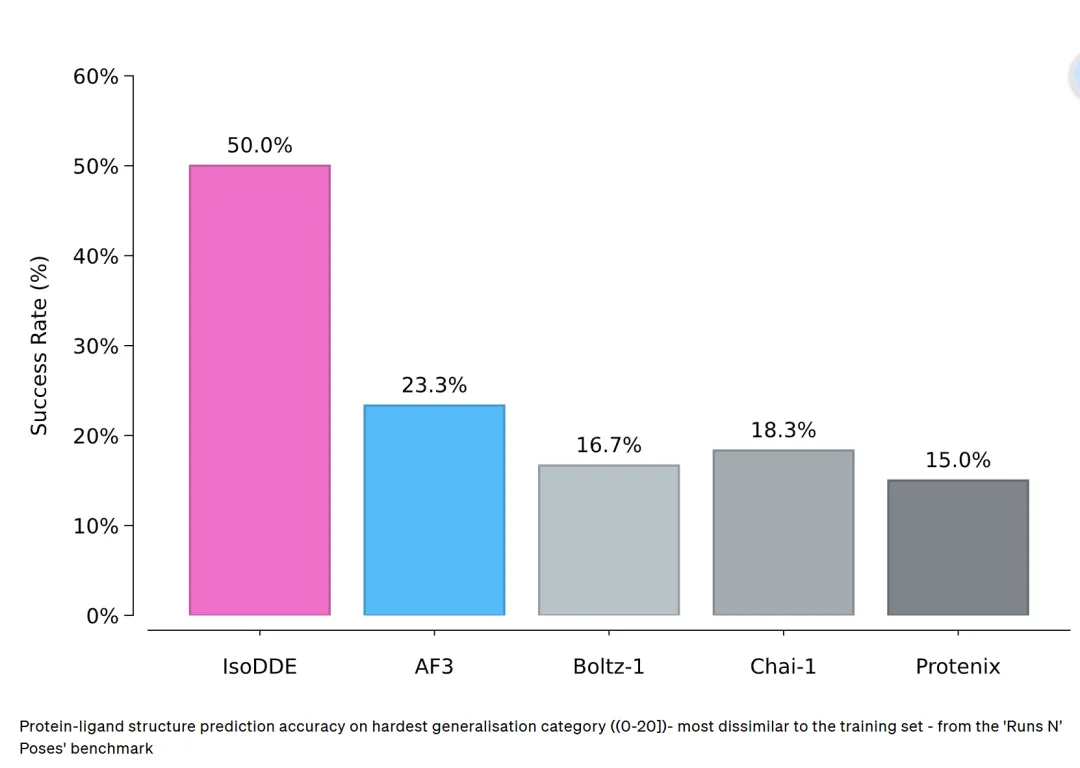
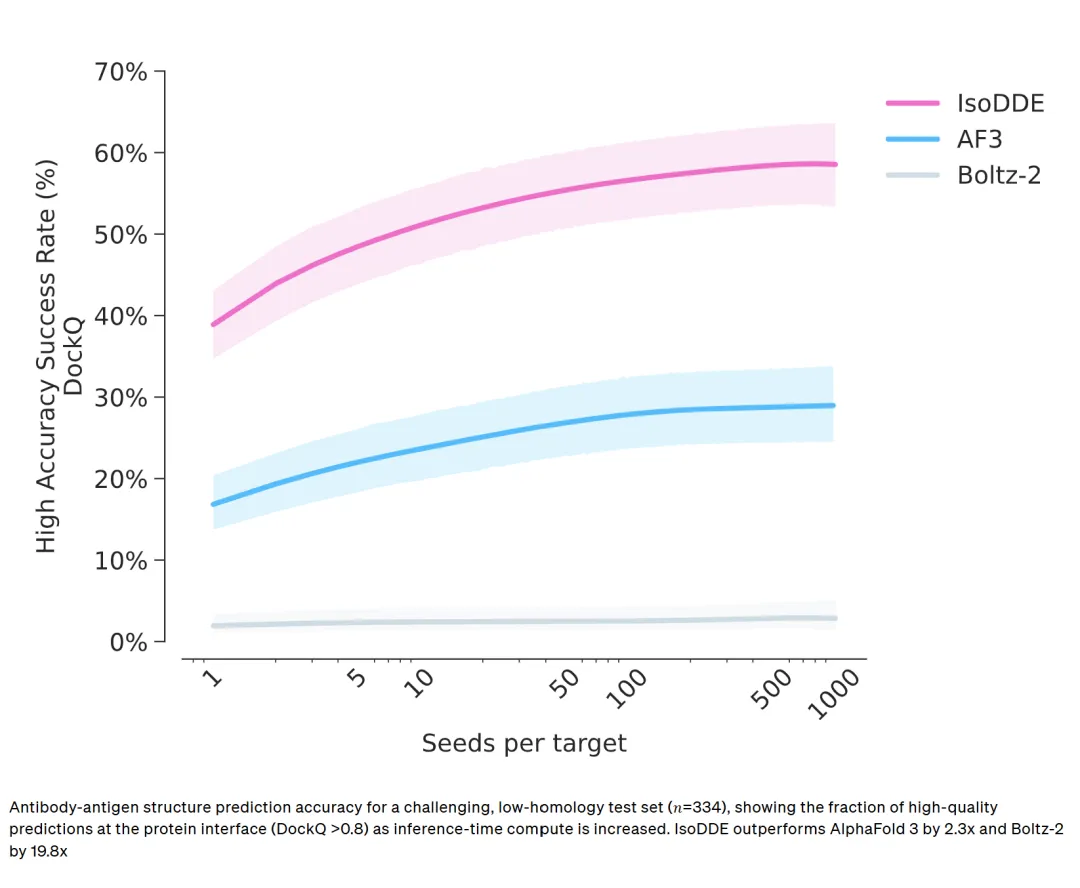
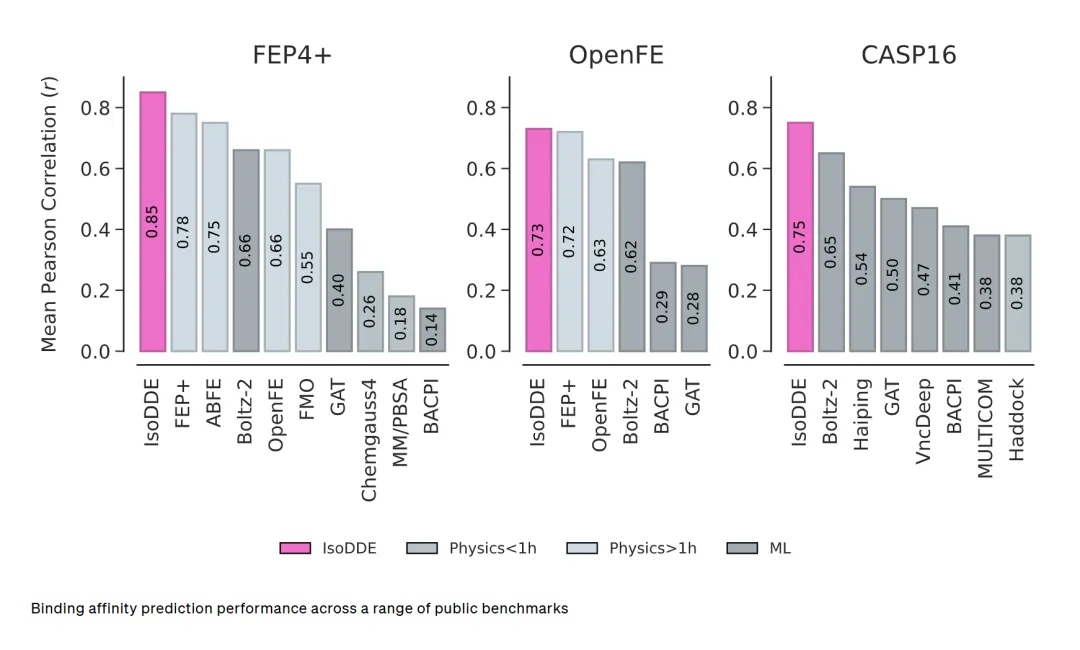
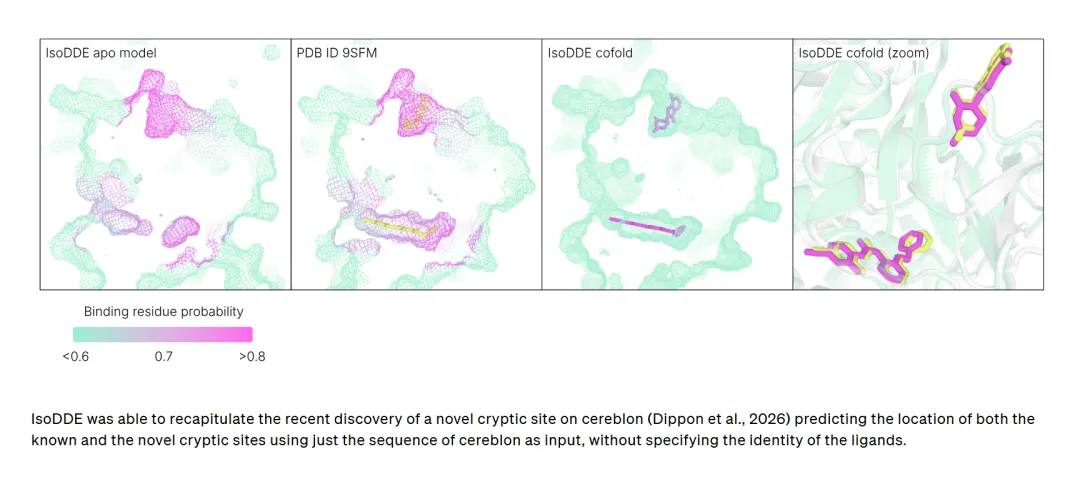
今天,我们很高兴向大家更新药物设计全新前沿领域的研发进展。我们在生物分子世界的预测精度上开辟了全新范式,依托前所未有的认知深度与精准度,实现了在计算机上理性设计全新药物的突破。我们首次公开Isomorphic Labs 药物设计引擎(IsoDDE)部分强大且全面的能力。这是一套一体化计算药物设计系统,预测精度全面超越 AlphaFold 3(AF3),填补了结构预测与实际药物研发之间的技术鸿沟。实测数据表明:在高难度蛋白 - 配体结构预测泛化基准测试中,IsoDDE 的准确率是 AlphaFold 3 的两倍以上;小分子结合亲和力预测精度超越传统物理金标准方法,同时耗时与成本仅为其零头;仅依靠氨基酸序列作为输入,就能精准识别靶蛋白上全新的潜在结合口袋。IsoDDE 为 AI 药物设计奠定了可规模化的技术底座,具备超高预测保真度,能够以史无前例的精度解析全新生物系统。自 2024 年我们与谷歌 DeepMind 联合发布 AlphaFold 3 以来,AI 药物发现行业发展日新月异。尽管 AlphaFold 3 相比前代结构预测模型实现跨越式升级,但仍存在核心短板:仅解析生物分子结构,不足以支撑计算机虚拟药物研发项目落地。合理药物设计是攻克人类疾病的关键,需要覆盖海量生化特性、分子相互作用的超高精度预测模型,且模型间可协同联动。更重要的是,生物与化学空间仍有大量未知领域待探索,模型必须具备超越训练数据集、泛化预测全新未知生物系统的能力。为攻克上述行业难题,我们正式推出自研IsoDDE 药物设计引擎,下文及技术报告将展示其核心能力。IsoDDE 三大核心能力:结构预测、口袋识别、结合亲和力预测。准确预测生物分子结构及其相互作用,是合理药物设计的核心基础。精准模拟蛋白几何结构的细微差异,可支撑下游多项关键研发任务:解析致病基因突变的影响、预测可与靶蛋白结合的候选分子等。AlphaFold 3 问世时重塑了蛋白 - 配体结构预测领域,其开源蛋白数据库已惠及全球 190 多个国家、超 300 万名科研人员。但基准测试发现:对于与训练样本差异较大的全新生物结构,AlphaFold 3泛化能力不足,而这类未知生物空间恰恰是药物研发最大的机遇与挑战所在。IsoDDE 在陌生蛋白 - 配体结构泛化预测能力上实现阶跃式提升。在专门测试全新口袋与配体泛化能力的 Runs N' Poses 基准测试中,针对难度最高的未知生物系统,IsoDDE 准确率达到 AlphaFold 3 的两倍以上。在最难泛化类别(与训练集相似度 0-20%)的蛋白 - 配体结构预测准确率:IsoDDE(50.0%)>AF3(23.3%)>Boltz-1(16.7%)>Chai-1(18.3%)>Protenix(15.0%)。案例验证:IsoDDE 可精准模拟诱导契合效应(蛋白为适配配体改变自身构型)、隐秘口袋开放(无配体时处于隐藏状态的结合位点)等复杂生物学机制,即便这些生物系统与模型训练集差异极大也能精准预测。典型案例:仅依托低相似度训练数据,IsoDDE 成功预测 NKG2D 同源二聚体界面隐秘口袋与蛋白互作抑制剂的结合结构;而同场景下 AlphaFold 3 预测失效。小分子药物(如阿司匹林)只是治疗手段的一部分。随着疗法向复杂生物药(如胰岛素)延伸,精准模拟抗体 - 抗原结合界面成为核心刚需。IsoDDE 在该领域精度实现大幅突破:在高难度低同源性全新抗体 - 抗原测试集上,高精度预测(DockQ>0.8)准确率较 AlphaFold 3 提升2.3 倍,较 Boltz-2 提升19.8 倍。尤其针对抗体最难预测、变异度最高的CDR-H3 环区,IsoDDE 表现尤为突出,彻底解锁从头设计抗体的全新可能性。掌握生物分子 3D 结构只是第一步,药物优化的核心是精准判断分子与靶蛋白的结合强度。传统预测方法存在两大痛点:要么仅适配与训练数据相似的化学空间,要么依赖超高算力、落地难度大(如物理建模法);近年深度学习方法速度更快,但精度始终不及传统物理方法。IsoDDE 在 FEP+ 4、OpenFE、CASP16 盲测结合亲和力三大权威基准测试中,大幅领先所有主流深度学习模型。更值得关注的是:IsoDDE 无需依托实验晶体结构,就能超越 FEP 等传统物理金标准方法。凭借高精度、极速预测的双重优势,IsoDDE 可助力科研人员在药物设计中快速筛选、优化不同化学系列的候选分子。无需已知配体,精准识别蛋白上所有潜在结合口袋,将开辟全新药物研发机遇:针对无结构注释的首创靶点、或为经典研究蛋白挖掘全新调控机制,通用口袋识别技术可穷尽分子设计的潜在作用机制。IsoDDE 仅依靠氨基酸序列,就能盲测识别全新可成药隐秘口袋,性能接近片段浸泡等传统实验技术;而传统实验耗时久、成本高,IsoDDE 仅需数秒即可完成计算机模拟预测。经典案例:脑啡肽蛋白(CRL4 E3 泛素连接酶复合物底物受体)近 15 年来,业界仅知晓沙利度胺经典结合口袋。2026 年科研实验首次发现其全新别构隐秘口袋。IsoDDE 仅输入脑啡肽蛋白序列,无需已知配体信息,就精准复刻了这一科研发现,同时定位经典口袋与全新隐秘口袋;指定配体后,还能精准模拟配体在对应口袋中的折叠与结合姿态。IsoDDE 在预测精度与功能维度上实现跨越式升级,深度解析人体生物分子运作机制,全面推进靶向药物设计研发进程。Isomorphic Labs 专业药物研发团队已将该引擎投入实际管线研发:解析未知生物分子结构、发现未被表征的结合口袋、设计全新化学分子,为患者研发突破性新药。我们将持续开拓计算机虚拟药物设计前沿,以更强的技术能力攻克传统难成药靶点。原文链接:https://www.isomorphiclabs.com/articles/the-isomorphic-labs-drug-design-engine-unlocks-a-new-frontier