由于保护对方版权和劳动成果,所以只选取了其中一节(涉及当天全部内容不到10%)的内容且只做总结,明天后天的会议更重要,有空的可以报名参加,报名地址和方式在文章最后。
总结如下:
本次发言以保障药品安全、推动生物医药产业高质量发展为目标,全面回顾 2025 年临床试验核查成效,明确 2026 年监管方向,并强调以数字化、智慧监管提升检查效能。
一、2025 年临床试验核查总体情况
注册核查提质增效,任务清零
新药注册核查:完成 394 项,核查通过率99.7%,任务存量清零、按时完成率 100%。 仿制药核查:完成 248 项,通过率98.8%。 共性问题:集中在知情同意、安全性报告、方案偏离、数据可靠性等环节,对严重问题予不通过、暂停试验、约谈、剔除数据等处置。 机构监督检查精准发力,监管穿透力增强
对 8 省 17 家机构、35 个专业开展不预先通知检查,覆盖化药、中药、生物制品、疫苗、儿童药。 重点核查机构质量体系与研究者责任,对严重数据问题不予注册,推动行业从 “点整改” 转向 “系统治理”。 境外检查与国际监管接轨
完成全球一类新药、仿制药境外临床试验核查,实现中国核查能力国际化突破。 2025 年我国接受 FDA、EMA 等境外检查 31 家次,中外监管关注重点趋同。
二、2026 年重点工作考虑
- 科学配置资源,强化核查与事中检查
持续高效开展注册核查,深化不预先通知的机构监督检查,完善风险处置与协同监管。 - 更新技术规范,统一标准引领
加快修订临床试验核查、机构检查要点与判定原则,接轨新版 GCP 与国际指南。 - 深化区域协同,建强检查员队伍
推进国家级 + 区域分中心 “一支队伍、一张网络、一套标准”,强化分层分类培训。 - 数字化技术驱动,智慧监管提质增效
建设智慧检查综合平台,运用AI 辅助研判、电子数据采集、智能风险评估、随机派检查员,实现全流程标准化、智能化。
三、核心目标
坚守受试者权益与数据真实可靠底线,以严监管促高质量创新,推动中国生物医药产业升级,助力中国创新药走向国际。
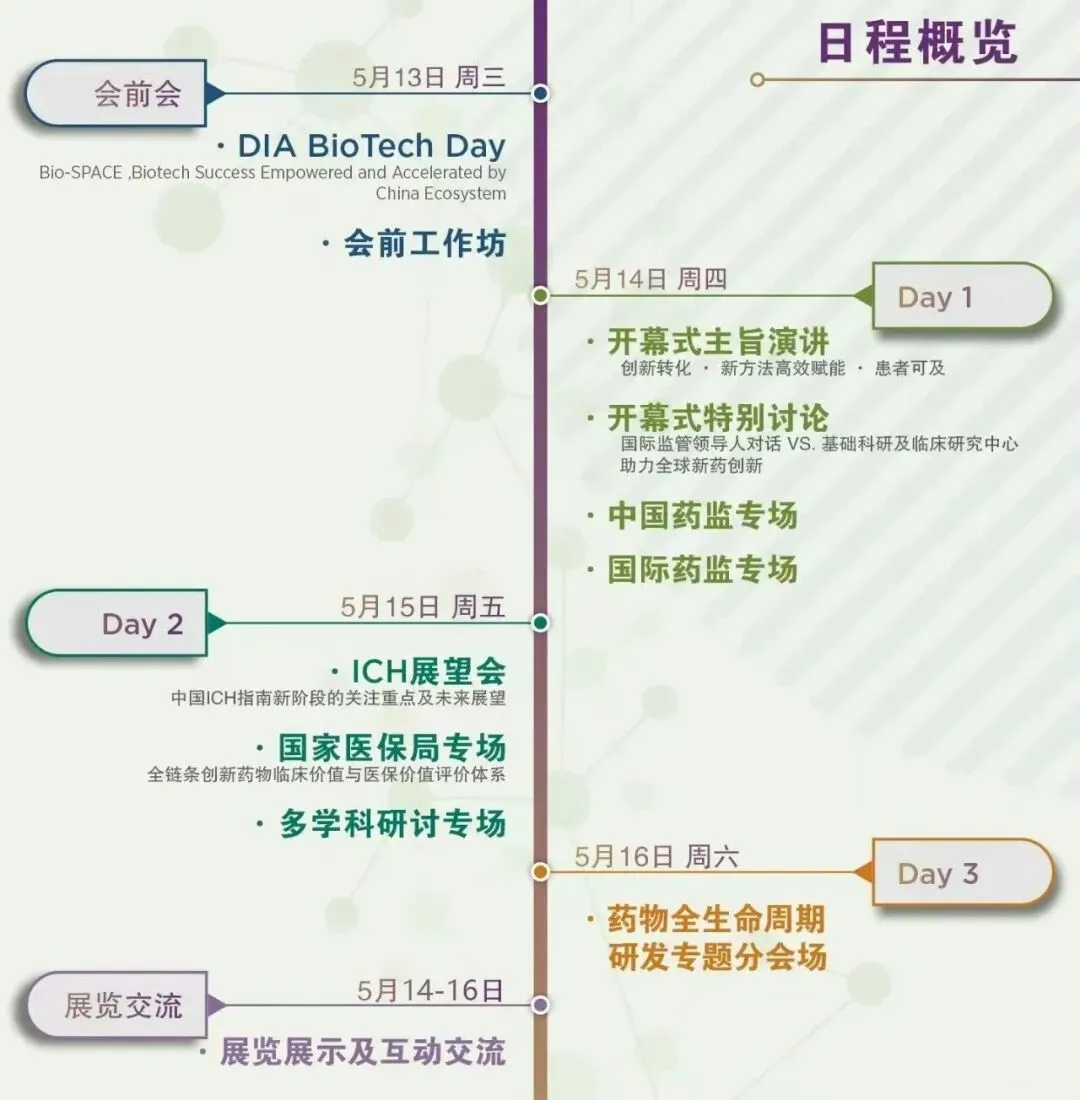
日程及注册报名
⬇️扫码查看初步日程

⬇️扫码注册参与