文章来源细胞闲聊等公开资料,转载请注明出处
818文件是什么?
2025年9月28日,国务院李强总理签署第818号令,《生物医学新技术临床研究和临床转化应用管理条例》正式落地,明确了“研究可转应用、医院可收费、技术可迭代”三大核心,按下了“细胞治疗”的加速键。
818号令正式出台,是近年来中国生物医药领域最具里程碑意义的法规事件 。它首次以行政法规的最高层级,系统地厘清了长期以来在监管实践中模糊不清的“药”与“术”的边界 。对于大量涌现的、以自体细胞疗法为代表的高度个性化、操作流程极其复杂、难以实现传统工业化量产的前沿技术而言,“华山一条路”的方法显得拥挤和不适。许多极具潜力的技术因为无法满足“产品”的标准化定义,而在商业化的门槛前徘徊不前。
818号令的智慧之处在于,它没有试图将所有创新都硬塞进“药品”的模具里,而是正视了生物医学技术的多元化特质,创造性地设计了第二条合规商业化路径。该条例明确,对于那些经过充分临床研究证明安全有效的生物医学新技术,就可以向国家卫生健康部门(NHC)申请“临床转化应用”,获批后即可作为一项正式的医疗服务项目在院内开展并合规收费 。这一路径的管理主体是NHC及其地方机构,其核心标的是“医疗技术服务”,而非标准化的“药品产品”。
这一制度设计改变了传统的游戏规则。它不仅为特定技术打开了通往市场的大门,更催生了全新的商业模式、合作关系和价值链条。对于细胞治疗企业而言,这不再是一个“是否要做临床试验”的问题,而是“要走哪条路来实现商业价值”的战略抉择。选择NMPA路径,意味着企业的目标是成为一个手握药品批准文号(MAH)的“产品制造商”;而选择NHC路径,则意味着企业可能需要转型为一个赋能顶级医院提供高精尖医疗服务的“技术服务商”或“整体解决方案提供商”。
这一抉择将直接影响企业的研发策略、融资规划、组织架构乃至企业文化。今天,我们就围绕这一核心抉择,展开系统而深入的探讨。
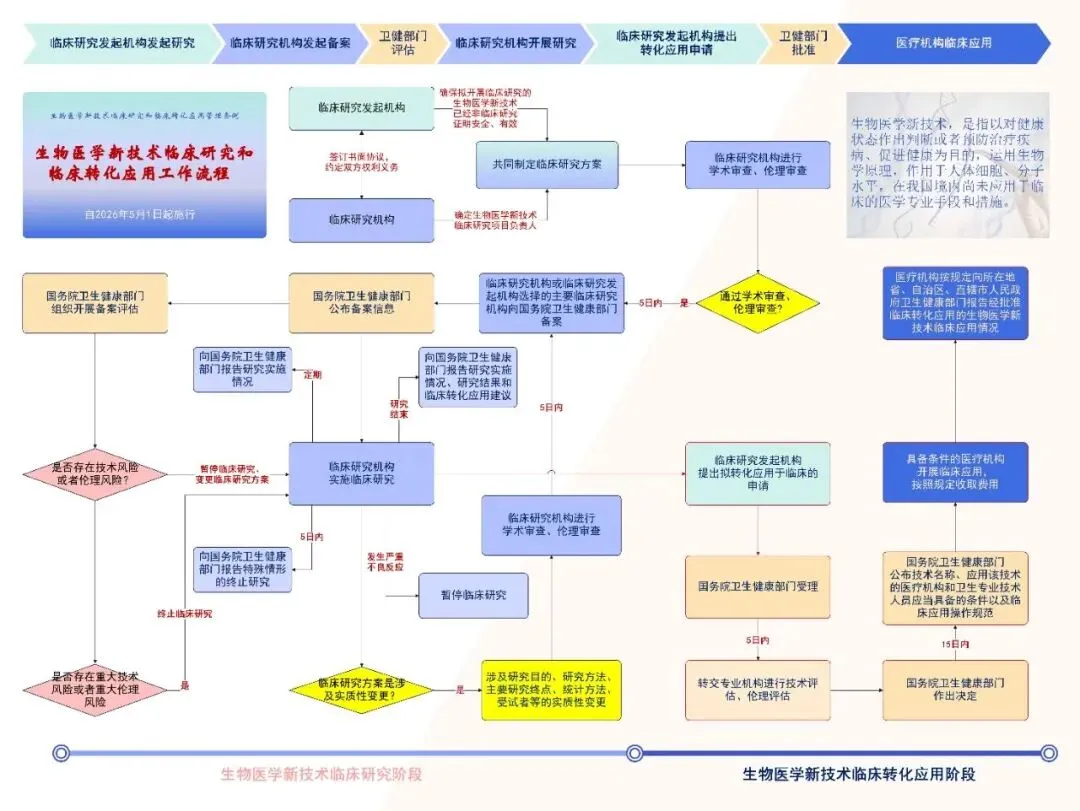
818文件对于生物医学新技术企业的深刻影响?
818号令所开辟的由NHC主导的“临床应用路径”,其最核心的价值在于为一类特殊的技术形态(高度个性化、操作流程复杂、难以大规模标准化、适用场景特殊等)提供了前所未有的商业化出口。对于致力于该类技术的生物医药企业,尤其是初创型生物技术公司(Biotech),NHC路径带来了三大战略性机遇:1) 加速商业化进程,优化现金流;2)提升企业估值与融资能力;3)维持“轻资产”运营,聚焦核心创新。
新路径的开启并非意味着一劳永逸,它对企业的战略能力、执行能力和合作模式提出了全新的、甚至更高的要求。1)精准路径判断与高质量研究的“硬门槛”;2)从“乙方”到“共同体”:医企合作模式的颠覆(共同设计研究方案、共建研发/制备平台、共享知识产权与收益、共同应对监管等);3)监管细节落地的不确定性。
《生物医学新技术临床研究和临床转化应用管理条例》(国务院令第818号)对企业的影响主要体现在以下几个方面:
1. 商业模式与路径选择
双轨并行机遇:企业可选择国家药监局(NMPA)主导的药品注册路径,或国家卫生健康委(NHC)主导的临床转化应用路径。前者适合标准化、可量产的技术,后者适用于高度个性化、操作复杂的前沿技术(如自体细胞疗法)。
路径选择挑战:企业需根据技术特点、资金实力和战略目标选择路径。NMPA路径需投入巨资建设GMP工厂,但可实现全国市场覆盖;NHC路径可加速商业化,但需与医疗机构深度合作,市场扩张速度相对较慢。
2. 研发与合规要求
临床研究规范:企业作为临床研究发起机构,需承担更多责任,包括非临床研究数据准备、临床方案设计、质量控制和风险管理等。需建立跨职能团队,确保研究符合法规要求。
合规成本增加:需投入资源建立全流程质量管理体系,包括供者筛选、物料管理、生产设施验证、分析方法开发等。同时,需确保临床试验数据的真实性、完整性和可追溯性,避免数据造假风险。
3. 合作模式与生态构建
医企深度合作:NHC路径下,企业需与医疗机构建立“利益共同体”,共同设计研究方案、共建研发平台、共享知识产权和收益。这对企业的商务拓展、战略合作和法律事务能力提出更高要求。
产业链协同:政策推动上下游企业协同发展,如病毒载体生产商、关键试剂供应商、专用设备制造商等上游企业,将受益于医院端对合规产品和服务的需求增长。
4. 融资与市场预期
估值与融资影响:通过NHC路径实现早期商业化的企业,可向投资人展示技术临床价值和商业潜力,提升估值和融资能力。但需注意,NHC路径下的收入模式(如技术服务费、耗材销售、收入分成)与传统药品销售收入模式不同,需合理评估市场预期。
行业洗牌与集中度提升:政策强化监管,淘汰不具备核心能力的企业,头部企业凭借技术、资金和合作优势,有望扩大市场份额,行业集中度可能进一步提升。
5. 国际竞争与合作
国际接轨机遇:政策推动与国际先进监管框架接轨,为企业产品出海创造条件。企业可通过建立符合国际标准的审评审批路径、生产质量体系和临床循证要求,提升国际竞争力。
技术合作与引进:政策鼓励创新,企业可通过国际合作引进先进技术和人才,加速自身发展。同时,需注意知识产权保护和合规风险。
6. 818号令是哪些主体细胞治疗行业的“斩杀线”?
1) 以大健康为目的的细胞治疗企业
818号令的实施将会对细胞治疗企业进行洗牌,以大健康为目的的企业将难有生存之路,目前监管相对宽松,随着《条例》的实施,各项执法政策的明确,以大健康为目的的企业将面临严重的生存压力,如果仍旧专注于大健康业务,所面临的风险成本非常高,因此818号令可以说是以大健康为目的的细胞治疗企业的“斩杀线”。
2) 缺乏核心竞争力的细胞治疗企业
短期而言,818号令对细胞药物开发企业是巨大利好,前期细胞药企的技术积累,可以利用新政策的便利,和符合条件的医院合作,经过备案然后公开收费,对细胞药企来说,是一个很好的出口。但从长期看,《条例》明确指出:临床研究机构可以自行发起生物医学新技术临床研究,这意味着具有实力的头部医院也可以做转化应用,公开收费。目前医院生存压力大,药物没有利润,生物医学新技术可以带来可观的收入,同时考虑生物医学新技术是未来发展方向,头部医院定会布局。对于普通的间充质干细胞,未经修饰的免疫细胞,这些技术壁垒相对较低,医院是可以完成的,加上医院本身掌握病源,如果病源量足以支持相应的成本,医院自己会实现自给自足,把相关的生物医学新技术变为“院内制剂”,如此以来,必将对生物药企产生重大影响。因此,长期来看,818号令也是缺乏核心竞争力的细胞治疗企业的“斩杀线”。
3) 大健康管理机构
目前细胞疗法是很多大健康管理机构的主要技术手段之一,818号令的实施,必定对其造成冲击,在健康管理机构将不能使用细胞产品,因此,818号令也是大健康管理机构的“斩杀线”。
4)部分销售人员
818号令规定,只有在三甲医院开展临床研究备案,证明安全性和有效性后,然后申报转化应用,获得批准后,才可以在医疗机构使用。这对市场销售人员会造成重大影响,不能再像当前一样推广,因此,818号令也是部分销售人员的“斩杀线”。
5)细胞产业上游供应链
细胞治疗作为前沿技术,虽然作为药品上市应用的产品还不是很多,但在某些方面已经得到广泛应用,尤其是健康保健方面。不得不说,当前细胞产品应用最多的领域还是健康保健,比如抗衰等,818号令的实施,必定会对健康保健的细胞应用造成影响,细胞用量的下滑,会传导到上游供应商,部分供应商的销售肯定会受影响,因此,818号令也是部分上游供应链的“斩杀线”。
结语
时间的指针,正在坚定地走向2026年5月1日。这无疑是一场严峻的考验,它将重塑行业的版图,决定未来谁主沉浮。
从“参与者”到“领跑者”的转变,非一朝一夕之功。这要求我们不仅要投入真金白银去建设厂房、购买设备,更要投入巨大的心力去重塑理念、再造流程、汇聚人才。这注定是一条艰难的荆棘之路,但也是通向顶峰的必经之路。
历史的机遇,总是垂青于那些有准备的头脑和有担当的行动者。那些真正将“责任”二字内化于心、外化于行,扎实构建起科学、质量、风控三大支柱的企业,必将穿越从实验室到病床的“死亡之谷”,成为中国细胞治疗产业化时代的领航者。
而他们所带来的,将不仅仅是商业上的成功,更是为千千万万翘首以盼的患者,点亮生命的希望之光。这,才是我们这个行业最崇高的使命。
总体而言,818号令为企业提供了更清晰的合规路径和商业化机会,但也对企业的战略规划、研发能力、合规管理、合作生态构建等方面提出了更高要求。企业需根据自身特点和市场定位,灵活调整策略,把握政策机遇,应对挑战。
请注明:姓名+研究方向!
END
作者 | Field
审核 | Sunbor
转载及其他广告合作请联系:13735420749(微信)
// 免责声明
* 创药邦内容团队专注于介绍生物创新药领域研究进展,本文仅作信息交流之目的,不代表平台立场;
* 本文仅供医疗健康专业人士学习参考之用,个人需向医疗健康专业人士进行咨询,以获得个人医疗建议;
* 本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及),不构成任何投资意见和建议,请以官方/公司公告为准;
* 如有涉及版权问题,请及时与我们联系,我们将给予删除或下线处理。


创药邦是面向生物创新药领域的专业平台,以「助力产业&资本」为己任。在创药邦,可以和同行分享最新的生物创新药前沿技术进展、行业政策和趋势,为创新药企提供融资、重组和并购等金融服务,帮助技术转化、项目转移和产品许可等产业服务,在创药邦找可靠的创新药项目,优化资源配置。


