据不完全统计,2026 年第一季度(Q1)国内细胞治疗赛道共有 17 家企业完成新一轮融资,融资金额超过 26 亿元。其中,亿元级融资 13 起,占比约 76%,原启生物、士泽生物、新景智源、吉美瑞生、英百瑞、莱芒生物这 6 家企业融资均在近 2 亿元及以上。高景气态势融资叠加可观融资金额再度验证了国内细胞治疗仍是生物医药资本配置的重要赛道,具有长期投资价值与产业发展韧性。
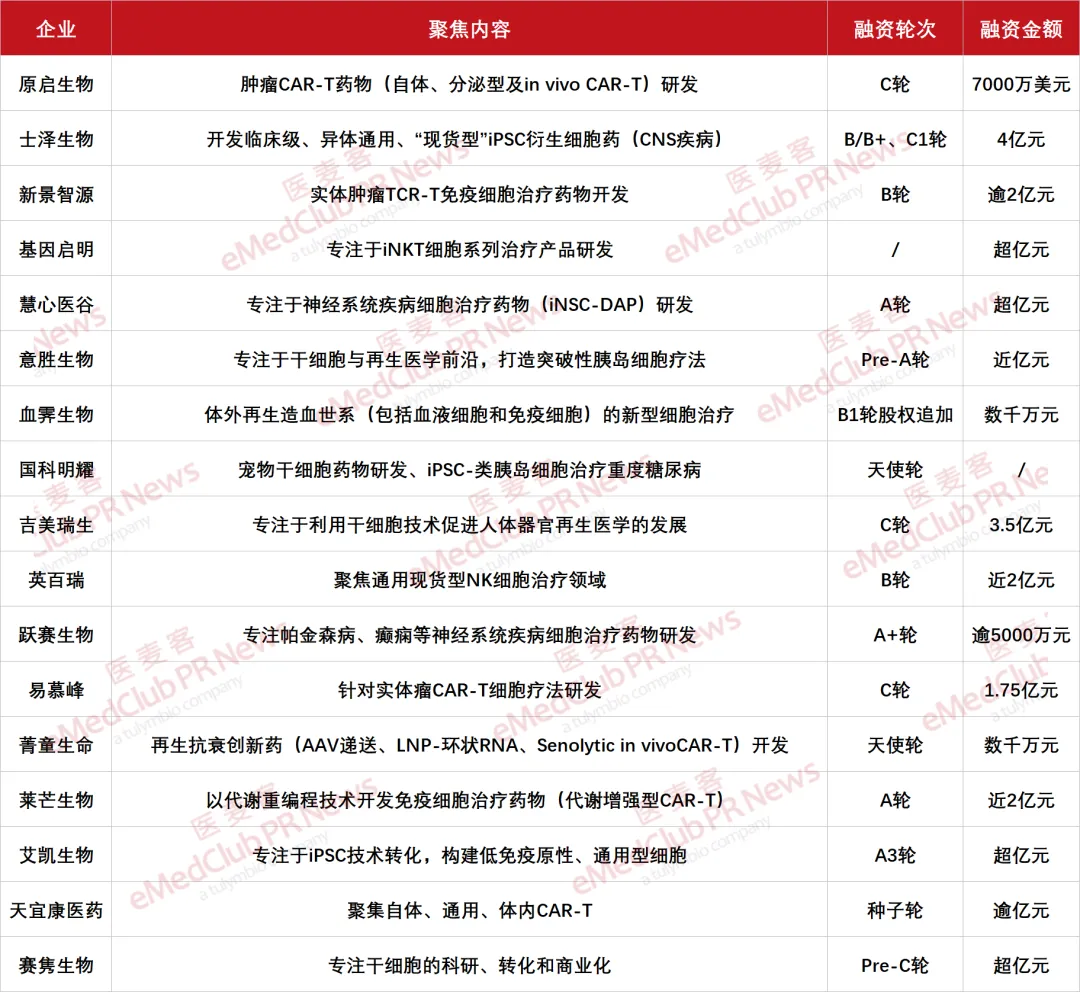
从应用场景来看,肿瘤治疗仍是细胞治疗赛道的核心需求,以 CAR-T、TCR-T 为代表的免疫细胞治疗持续向实体瘤攻坚,in vivo CAR-T、代谢增强型 CAR-T 等下一代技术不断迭代;iPSC 技术成为通用型、现货型细胞药的核心支撑,在神经退行性疾病、代谢疾病等领域实现多点突破;干细胞疗法则在器官再生、慢病管理等场景加速商业化落地;宠物细胞药、再生抗衰等新兴方向也获得资本持续关注,应用场景不断丰富,为行业发展打开全新增长空间。
从融资轮次分布来看,跨度范围广,从种子轮/天使轮到 A 轮,再到 B 轮和 C 轮均有,资本对早期项目及成长期项目各有偏好。其中,种子轮、天使轮共 3 起,覆盖宠物干细胞药物、再生抗衰创新药、体内 CAR-T 等前沿创新方向,资本注重差异化布局和源头创新;Pre-A 轮、A 轮、A + 轮、A3 轮共 5 起,聚焦 iPSC 技术转化、干细胞疗法、代谢增强型 CAR-T 等具备临床潜力的项目。
B 轮及以后共 8 起,这些企业大部分依托已验证的技术平台与临床管线,获得大额融资加速管线临床验证、国际化、商业化筹备。
原启生物
核心管线 Ori-C101 是一款靶向 GPC3 用于治疗晚期肝细胞癌(HCC)的自体 CAR-T 候选药物,即将开展关键临床 II 期试验,有望成为全球首款获批的针对肝细胞癌的 CAR-T。当下尚无针对实体瘤的 CAR-T 获批上市,大额融资是资本对其核心管线未来商业价值的押注,以及对原启生物下一代 CAR-T 布局的认可。
士泽生物
自主开发了治疗帕金森病、脊髓损伤、渐冻症等具有明确未被满足临床需求的重大或危重神经系统疾病的「中国首发」或「全球首款」临床级 iPSC 衍生神经细胞治疗新药。据最新官网消息,已经获得 NMPA 和 FDA 正式批准的九项中美注册临床试验批件。
吉美瑞生
吉美瑞生聚焦慢性阻塞性肺病、特发性肺纤维化、慢性肾脏病,其 REGEND001 管线临床进展处于全球领先行列,并且已经在海南博鳌乐城国际医疗先行区启动三项「临床转化应用」项目,核准治疗费用为 15 万元/次。截至 2 月,已为 140 余位患者成功提供了再生疗法,初步验证了其商业化潜力。
易慕峰
CLDN18.2 CAR-T 管线 IMC002 已经启动 III 期确证性临床研究,位列同靶点 CAR-T 进展第一梯队,也布局了 in vivo CAR-T 方向,管线梯度合理、临床推进高效,叠加已向港交所主板递交上市申请,具备强劲的商业化落地潜力。
赛隽生物
手握「全球同适应症进度第一」和「全球首个」的管线,慢加急性肝衰竭、缺血性脑卒中、肝损伤、肌少症等管线已分别在南沙等先行先试区域获批落地,相关项目已开展收费治疗并产生实际收入,是目前为数不多实现干细胞临床治疗商业化落地的企业。
以上 5 家完成 Pre-C 轮/C 轮融资的企业均已跨过早期技术验证阶段,进入临床价值与商业化潜力双重兑现期,共同具备吸引资本的关键特质:
一是管线具备全球或国内领先的临床进度,多款产品瞄准实体瘤、神经退行性疾病、器官损伤等未被满足的重大临床需求,部分有望成为全球或中国首款获批产品,具备差异化壁垒;
二是战略布局清晰,技术平台具备延展性,在下一代 CAR-T、iPSC 通用型细胞、体内递送等前沿方向均有布局,形成可持续迭代的管线梯队;
三是商业化路径明确且已有初步验证,部分企业在医疗先行区实现收费治疗、产生实际收入,证明产品具备真实市场需求与变现能力。
整体而言,2026 年第一季度的细胞治疗赛道,呈现出「多轮次覆盖、应用场景延伸、技术差异化」的良性发展态势,17 家融资企业各有侧重、协同发力,勾勒出国内细胞治疗产业的发展轮廓,随着资本的注入,将为行业未来持续释放长期价值,形成高质量发展态势提供强大助力。
参考资料:
1.企业官网及公开消息
PEIpro® 系列产品
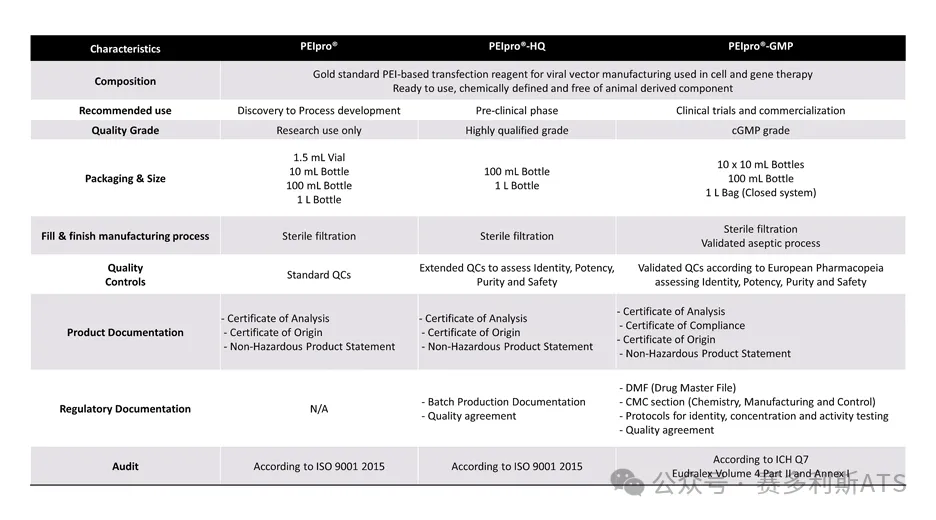
PEI的生产遵循非常严格的质量控制和法律法规,有三个质量等级:研发级的PEIpro®用于工艺开发,更好质量等级的PEIpro®-HQ用于临床前研究和早期临床试验,最高质量等级即完全GMP级别的PEIpro®-GMP可用于临床病毒载体的生产(包括慢病毒,腺病毒,腺相关病毒等),满足细胞治疗和基因治疗的质量和监管要求。
专为悬浮体系生产AAV开发的
FectoVIR®-AAV
FectoVIR®-AAV 是新一代转染试剂,专为在悬浮和贴壁 HEK-293 衍生细胞体系中大规模生产rAAV而开发。FectoVIR®-AAV转染试剂保证更高的 rAAV 滴度,提高大规模生产的可放大性,拥有药品GMP级产品降低生产工艺的风险。FectoVIR®-AAV GMP级产品在经过验证的无菌工艺下生产,符合 ICH Q7、GMP指南第二部分。
与PEIpro®和其他竞争对手相比,FectoVIR®-AAV 在悬浮细胞中能生产更高滴度的rAAV病毒载体。与其他竞争对手相比,FectoVIR®-AAV可重复性地大幅提高 AAV 产量,可高达10 倍。
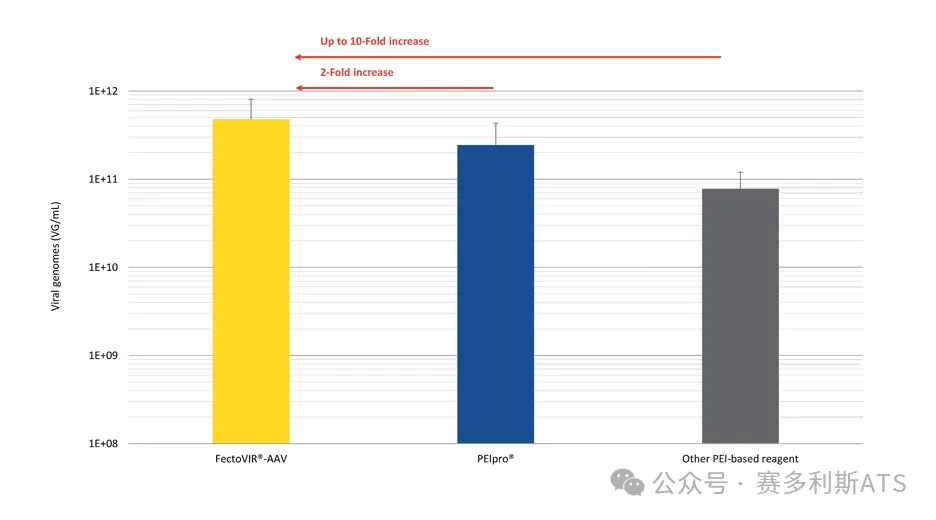
和竞争者相比,FectoVIR®-AAV 可提高rAAV-2-GFP的滴度达10倍。按厂家推荐条件进行转染,72小时后收取病毒。
大规模瞬时转染需要在给定的时间范围内将大量转染复合物添加到悬浮细胞中。FectoVIR®-AAV 经过优化,可将复合物体积降低至1%,转染复合物的稳定性提高到3小时,易于转染复合物的转移和工艺放大。
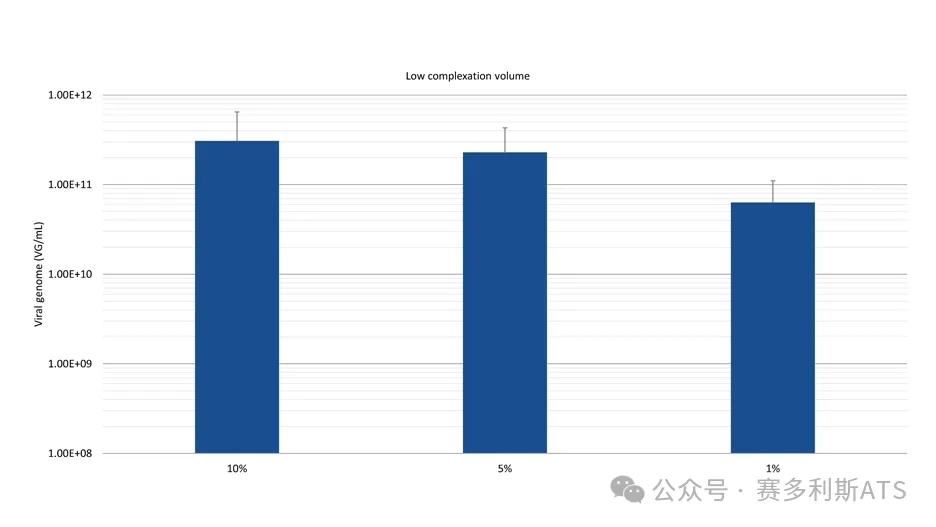
使用FectoVIR®-AAV制备不同体积的转染复合物:最终培养体积的10%,5%和1%。转染后72小时使用qPCR定量检测。
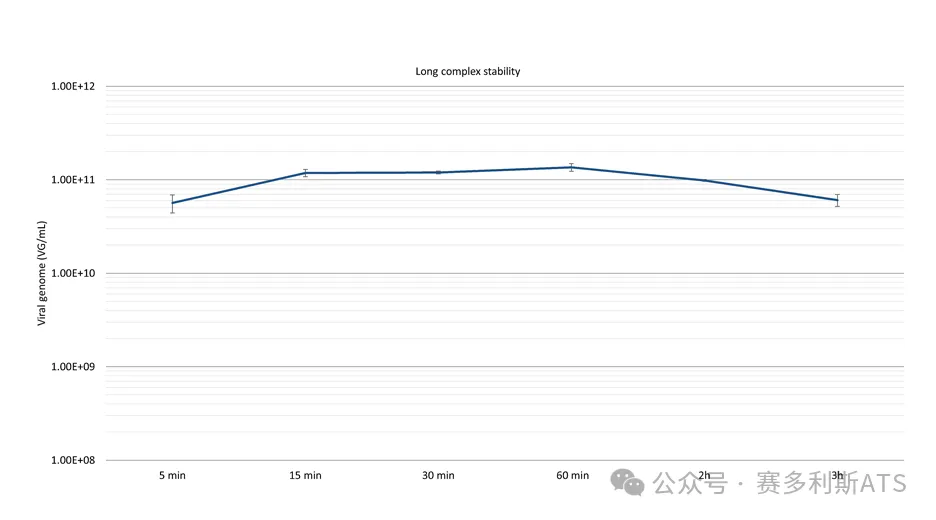
按厂家推荐条件进行转染,使用不同的复合物孵育时间(15分钟到3小时)。 转染后72小时使用qPCR定量检测。
FectoVIR®-LV
慢病毒载体被认为是同种异体或自体细胞疗法(如CAR-T)的首选载体。细胞治疗生产商通常使用瞬时转染系统生产这些载体,在工艺开发阶段进行放大。FectoVIR®-LV是下一代转染试剂,不含动物源成分,专为在HEK-293系统中提高LV的产率而设计。使用FectoVIR®-LV可以增加每批次生产的剂量数,以治疗更多的患者,同时降低生产成本。
与其他市售用于慢病毒生产的转染试剂相比,FectoVIR®-LV可提高功能滴度达3倍。
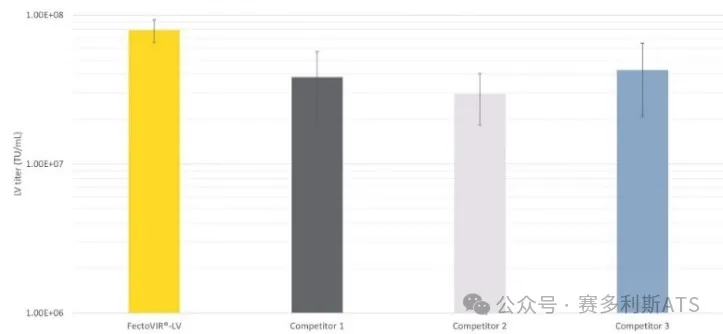
与慢病毒生产领域的竞争者相比,FectoVIR®-LV表现出高产率。
FectoVIR®-LV在提高生产率的同时DNA用量可以减半。为了支持我们的客户,赛多利斯ATS提供了全面的DOE服务,以优化转染步骤的关键参数,达到更高的滴度。
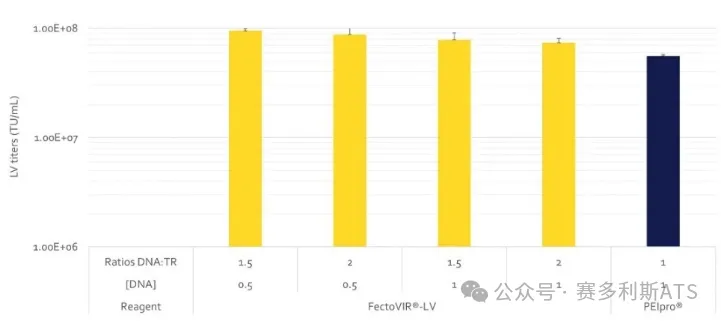
FectoVIR®-LV转染方案使用更少量的DNA并优化滴度,以提高工艺经济性。
大规模瞬时转染的挑战包括在最佳时间范围内转移转染混合物。如果转染试剂不适合大规模生产,这一步骤可能成为一个限制。FectoVIR®-LV为大规模生产而设计,可减少复合物体积并提高复合物稳定性, 从而有足够的时间将混合物转移到大型生物反应器(>200 L)中。使用推荐的5%复合物体积和30分钟的复合物孵育时间,FectoVIR®-LV证明了其高效性,该条件可以进一步优化以符合您的工艺。赛多利斯ATS建议使用适合您系统的DOE研究。
赛多利斯先进治疗
赛多利斯是国际领先的生物制药行业的合作伙伴,致力于帮助细胞和基因疗法开发人员生产和商业化其先进治疗药物产品(ATMPs)。在过去十年中,公司通过收购互补的先进治疗耗材、服务和技术(从质粒工程和制造到细胞培养基、试剂和整体柱层析),扩展了其传统的一次性生物工艺解决方案。赛多利斯先进治疗解决方案旨在通过提高生产力、改善工艺经济性以及支持安全合规的生产来克服当前的生产挑战。赛多利斯产品目前用于已获批的细胞和基因疗法,并积极支持全球临床管线。对创新解决方案的持续投资表明其致力于推动该领域的发展并使这些挽救生命的治疗方法成为现实。
扫描二维码添加官方微信
获取更多的产品知识和最新资讯!


