
2026年4月9日至12日,第93届中国国际医疗器械博览会(CMEF)在上海国家会展中心举行。作为“十五五”开局之年首场行业大展,本届CMEF以“创新聚变·无限跃迁”为主题,吸引全球近5000家品牌企业参展。

展会期间,翔康医学携一站式CDMO+CRO服务能力亮相,与来自国内外的医疗器械企业、临床专家及产业伙伴进行了深入交流。来访者重点关注三类合作方向:创新器械的研发设计外包、临床试验方案优化、以及多市场同步注册的策略支持。翔康医学结合具体案例,就不同产品类型的开发周期、注册路径选择、生产落地可行性等实际问题进行了现场沟通。



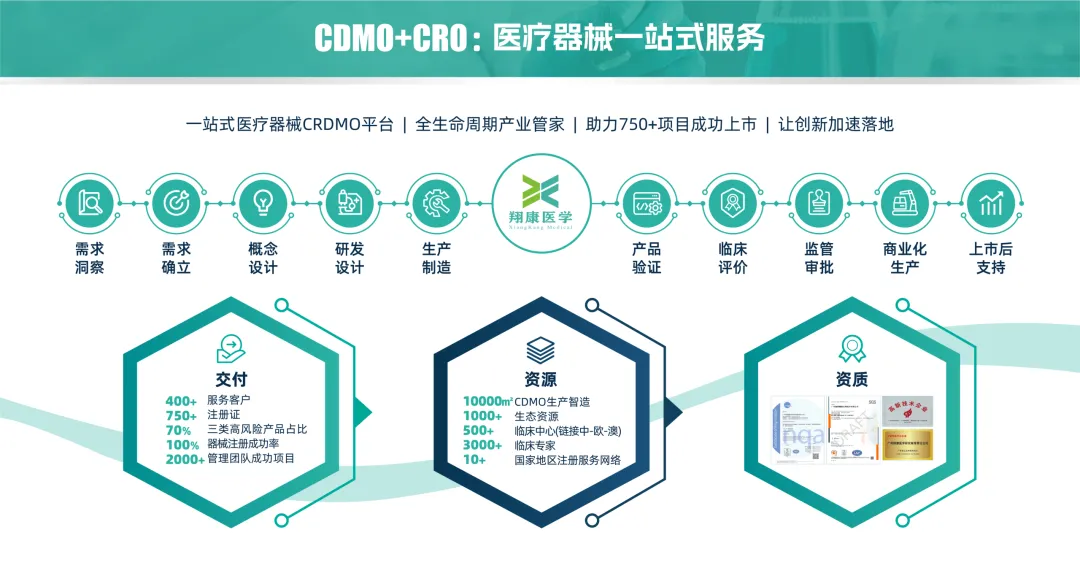
在医疗器械创新加速、注册监管日趋规范的背景下,从研发到上市的全周期服务能力成为行业关注重点。翔康医学围绕“研发转化、临床研究、全球注册、生产智造”四大板块,展示了在CRO(合同研究组织)、CDO(合同设计组织)、CMO(合同生产组织)协同服务方面的实践成果。
展位现场重点呈现了翔康在创新医疗器械领域的服务案例:截至目前,翔康已累计取得750余张注册证,其中三类器械占比超过70%;创新器械注册成功率达100%,累计获证超50张。这些数据反映了翔康在复杂器械、高风险品种以及创新产品申报上的经验积累。
同时,翔康依托覆盖中国、欧洲、澳大利亚的临床研究网络,以及总面积超10,000平方米的双中心多产线CDMO基地,可为客户提供从样品到商业化生产的全链条支持。公司已通过ISO 9001及ISO 13485双体系认证,服务能力覆盖全球10余个国家和地区的注册申报。
四天的展会已落幕,但产品从概念到市场的长链条仍在加速运转。翔康医学将继续聚焦医疗器械产业转化中的关键节点,在研发设计、临床评价、合规注册与委托生产等环节提供稳定、可追溯的服务支持。面向未来,翔康将依托现有双中心产能及全球化临床资源,进一步提升对创新器械、高风险品种及海外注册需求的响应能力,与行业伙伴共同推动优质医疗器械产品安全、高效地走向市场。
期待下一次CMEF,与您再会。







