引言
RNA寡核苷酸的治疗研究可追溯至1978年,当时研究者首次证实反义RNA能够通过碱基互补配对结合靶mRNA,从而抑制蛋白质的合成,这一突破性发现为寡核苷酸治疗的发展奠定了坚实基础。此后数十年,科研工作者持续致力于改进RNA寡核苷酸的化学合成方法,通过优化核苷酸骨架结构、修饰碱基或核糖等方式,不断提升其体内稳定性、靶向性与生物利用度,推动寡核苷酸治疗从理论走向实践。20年前,小干扰RNA的发现进一步点燃了全球范围内RNA化学研究的热情,该技术可通过诱导靶RNA降解实现高效的基因沉默,其开创性意义也使其相关研究者荣获诺贝尔奖,极大地推动了RNA治疗领域的跨越式发展。

核酸药物

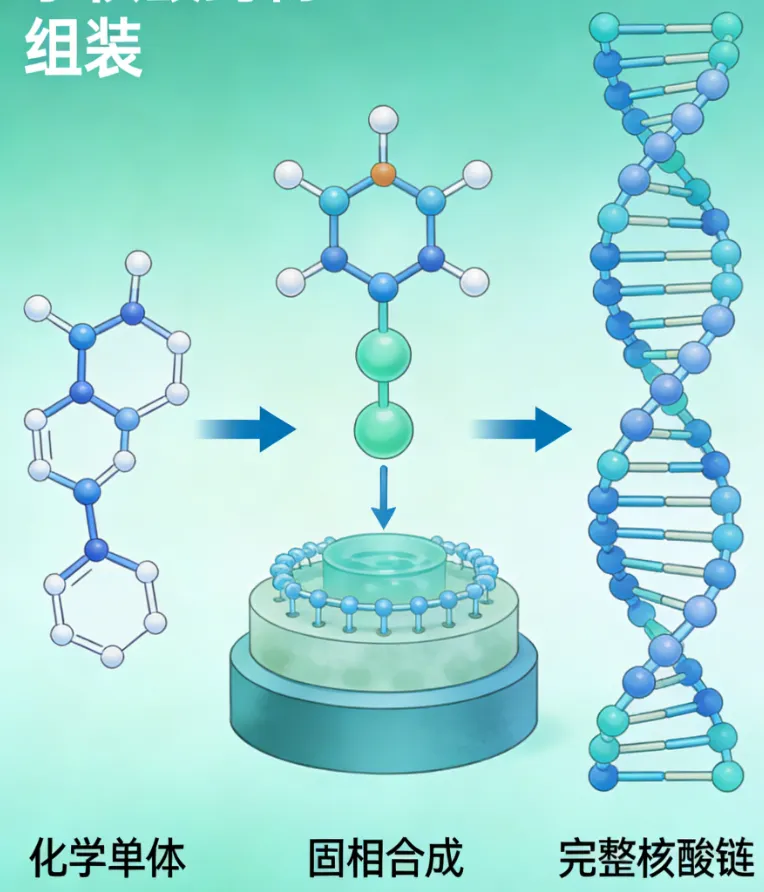
亚磷酰胺法是有机化学与生物医药领域的重要分支,核心围绕亚磷酰胺类化合物的结构、反应特性及应用展开,尤其在RNA寡核苷酸固相合成中发挥着不可替代的核心作用,是推动核酸药物工业化生产的关键技术支撑。
固相合成的本质是亚磷酰胺单体迭代的化学。接下来以一个标准磷酸二酯骨架的合成为例,拆解每个步骤的分子机制。
01
脱保护(Detritylation)
该步反应的主反应是酸催化下的SN1裂解,常用的4,4‘-二甲氧基三苯甲基(DMT)保护基,使用三氯乙酸或二氯乙酸(DCA)溶剂(如二氯甲烷)溶液。
DCA的质子(H⁺)攻击DMT基团与糖环5‘-氧原子之间的醚键(O-CH₂-),使该键极化、弱化。该C-O键发生异裂,其发生SN1型裂解,生成稳定的三苯甲基碳正离子(呈橙色)和自由的5‘-羟基。由于生成的三苯甲基碳正离子具有极高的稳定性(得益于三个苯环的共轭分散电荷)。DMT基团以稳定的碳正离子形式离去。
产物为暴露出自由的5‘-羟基,这是下一轮偶联反应的亲核中心。
监测点:生成橙黄色的DMT⁺碳正离子,其在495 nm处有强吸收,是实时监测的物理基础。
该反应条件温和,选择性高,不会裂解碱基上的酰胺保护基(如Bz, iBu)或糖环2‘位的硅基保护基(如TBDMS)。
副反应:脱嘌呤及其连锁,这是限制合成链长和影响产物纯度的最主要副反应,尤其在合成长链或富含嘌呤(A, G)的序列时。在酸性条件下,嘌呤碱基(腺嘌呤A、鸟嘌呤G)与脱氧核糖之间的N-糖苷键变得不稳定。强酸(如TCA比DCA更强)或过长的脱保护时间会催化该键断裂,导致碱基丢失,在糖环上留下一个不稳定的缺碱基位点。在后续的氧化步骤中,碘和弱碱(吡啶)的环境会使这个不稳定的缺碱基位点发生β-消除反应。导致磷酸二酯骨架在缺失碱基的核苷酸处彻底断裂,生成两条短链。最终产物中会出现一系列比目标链短的缺失序列杂质,难以纯化分离。
主要过程控制方法:
试剂选择:优先选用二氯乙酸而非更强的三氯乙酸,在保证足够脱保护速度的同时,尽可能降低酸强度,减少脱嘌呤风险。
时间控制:精确控制酸与树脂的接触时间(通常15-30秒),确保DMT刚好完全脱除,但又不至于长时间浸泡引发副反应。
实时监测:通过在线UV检测器监测495 nm处的吸光度。每循环释放的DMT⁺量应与树脂上活性链的数量成正比。若某一步吸光度显著下降,直接表明上一步的偶联效率低,链没有成功延伸,为即时工艺诊断提供了最关键的数据。
洗涤:脱保护后立即用惰性溶剂(如乙腈)充分洗涤,迅速移除酸性环境和DMT⁺离子,终止反应。
02
偶联(Coupling)、缩合
偶联反应的本质是 5‘-羟基对活化磷中心的亲核取代。我们以最常用的 四唑 作为活化剂, 2‘-氰乙基-N,N-二异丙基亚磷酰胺 作为单体活性基团的标准结构进行说明。
单体的活化(生成高活性磷中间体):唑的酸性质子与亚磷酰胺单体(如 5‘-DMT-2‘-OMe-I-CE Phosphoramidite)中三价磷上的氮原子结合,形成良好的离去基团(质子化的二异丙胺)。磷原子被亲核进攻,形成高活性的四唑磷中间体。此步将单体从稳定的储存形式,转化为一个具有强亲电性的磷中心,迫切等待与亲核试剂反应。
亲核取代与链延伸(SN2机制):一步暴露的链末端5‘-羟基氧原子,作为亲核试剂,进攻活化的磷中间体,发生SN2型取代反应,5‘-氧原子与磷原子形成新的P-O键的同时,磷原子上连接的四唑基团作为离去基团被脱去。释放出四唑和二异丙胺,生长链的5‘-氧与单体的3‘-磷之间形成了不稳定的亚磷酸三酯键。
产物为新形成的键是三价磷的亚磷酸三酯,非常不稳定,必须在后续的氧化步骤中转化为稳定的五价磷(磷酸酯或硫代磷酸酯)。
关键点
根据化学平衡和质量作用定律,要使树脂上近乎100%的链末端都发生反应,必须使用大大过量的单体(通常为树脂载量10-50倍)。这是实现 >99.5% 偶联效率的物理化学基础。
活化剂的选择决定反应性:四唑适用于大多数单体。5-乙基硫代-1H-四唑:酸性更强、活性更高,常用于活化空间位阻大的单体(如2‘-O-甲基、LNA等修饰单体),或用于合成长链、困难序列,以缩短偶联时间、提高效率。
水是此反应最致命的杀手。水分子(H₂O)是比5‘-羟基更强的亲核试剂。它会迅速淬灭活化的单体,生成水解副产物(H-膦酸酯),导致该轮次偶联完全失败。因此,溶剂和系统的绝对无水是工艺控制的重中之重。
必须提供足够的时间让过量的活化单体扩散至树脂的所有活性位点并完成反应。对于长链或高载量树脂,需要优化流速和混合以确保传质充分。
监控点
偶联步骤本身没有直接的在线监测方法。其效率是通过下一步脱保护时释放的DMT量来反向计算的。如果某一步偶联失败,该链末端仍带有DMT,在下轮脱保护时就不会释放DMT⁺,导致监测到的吸光度下降。
稳定性与反应性:单体本身在无水条件下可长期储存(稳定性),但在活化剂作用下能瞬间转化为高活性中间体(反应性)。
高效与专一:反应速度快、效率极高,且主要发生在5‘-OH上,对其他保护基(如碱基上的酰胺、2‘-位的硅醚)基本无影响。
模块化与灵活性:任何碱基或糖环修饰,只要能制成相应的亚磷酰胺单体,就能无缝接入这套流程。
03
封端(Capping)、带帽
封端反应的本质是 乙酰化反应。使用 乙酸酐 作为酰化试剂,N-甲基咪唑 作为高效催化剂。N-甲基咪唑是强亲核催化剂。它首先攻击乙酸酐,形成高活性的 乙酰基咪唑鎓中间体。这个中间体极其活泼,能迅速与任何游离的5‘-羟基反应,生成稳定的 5‘-O-乙酰酯。
被乙酰化的链末端失去了亲核能力,在后续所有合成循环中再也无法与任何单体偶联。它的长度就此固定,最终成为比目标全长链短一个或多个核苷酸的 “n-1”, “n-2” 等缺失序列杂质。
可能存在的修复
在偶联步骤中,高活性的亚磷酰胺单体有极小的概率(但确实存在)不仅攻击5‘-羟基,还会攻击鸟嘌呤碱基上的 O6位氧原子,形成一种不希望的O6-磷酰化副产物。
修复原理:封端试剂中的 乙酸酐/N-甲基咪唑 同样可以乙酰化这个O6位加合物上的磷中心。被乙酰化后,这个不稳定的结构在后续的氧化步骤和最终的氨水切割/脱保护步骤中会被水解清除,从而防止它最终成为难以定性的复杂杂质。
封端是固相合成工艺中杂质控制策略的核心。
如果不封端:本轮未反应的游离5‘-OH,会在下一轮合成中“复活”,与新的单体偶联。这样会产生一系列长度只差一个碱基、但序列不同的“失败链”。它们与目标全长链的物理化学性质(如极性、分子量)极为相似,通过HPLC或电泳极难分离,会严重降低最终产物的纯度。
封端之后:这些失败链被永久“冻结”。它们全部变成比目标链短,且末端是乙酰基的杂质。这些杂质与目标全长链的差异更明显,在后续纯化(如离子交换色谱、反相色谱)中更容易被分离去除。
控制
试剂有效性:必须使用新鲜或妥善保存的乙酸酐和N-甲基咪唑,确保其高活性。
反应时间:通常很短(15-30秒),因为反应非常迅速。
配比:标准的封端试剂是乙酸酐、N-甲基咪唑和某种溶剂(如四氢呋喃或乙腈)的混合溶液,其配比经过优化以确保快速、完全的乙酰化。
无需实时监测:封端步骤本身没有直接的在线监测。其有效性是通过最终产物的杂质谱分析来间接验证的。如果封端不完全,最终HPLC图谱中会出现异常的、难以解析的连续缺失峰。
04
氧化(Oxidation)
氧化步骤的目的是将偶联后形成的、化学上不稳定的 三价亚磷酸三酯 键,转化为稳定的 五价磷 骨架。根据最终所需骨架类型,分为 氧化 和 硫化。
使用碘(I₂)、水(H₂O)和弱碱(如吡啶) 的混合物。三价磷(亚磷酸酯)被碘(I⁺)氧化。水分子提供氧原子,最终将不稳定的亚磷酸三酯转化为稳定的磷酸三酯。
若需引入硫代磷酸酯键,则用Beaucage试剂或EDITH等硫化剂替代碘溶液。硫原子来自硫化剂,形成硫代磷酸三酯。
如果氧化不完全,残留的亚磷酸酯键在后续的 氨水切割/脱保护 步骤中(碱性条件)会发生 水解和β-消除反应,导致寡核苷酸链在未完全氧化的位点发生断裂,产生短链杂质。碘和水的氧化体系具有一定的酸性。与脱保护步骤类似,在氧化过程中,如果条件控制不当(如时间过长),也可能加剧嘌呤碱基(A、G)的脱除。
确保使用新鲜配置的氧化试剂,并提供足够的反应时间(通常30-60秒)。精确控制氧化时间,避免不必要的延长。
05
循环结束
用乙腈彻底洗涤,完成一个核苷酸的添加。重复循环N次,即得长度为N+1(含起始核苷酸)的寡核苷酸-树脂复合物。
结
最终切割与脱保护
使用浓氨水/甲基胺溶液,加热(通常55-65°C)。
β-消除:氨水中的氢氧根离子攻击磷酸三酯上氰乙基保护基的β-氢,发生消除反应,脱去丙烯腈,生成磷酸二酯阴离子。
酰胺水解:碱基上的保护基(如苯甲酰基、异丁酰基)被氨水水解,释放出游离的氨基。
酯键切割:氨水水解连接臂的琥珀酸酯键,将完整的寡核苷酸链从树脂上释放。
看完这篇,是不是对小核酸药物的合成是否有了更清晰的认知?
后续我们还会聊聊小核酸相关内容,记得关注哦~

