片剂线增加胶囊剂,生产许可申报新增生产线还是生产线变更?
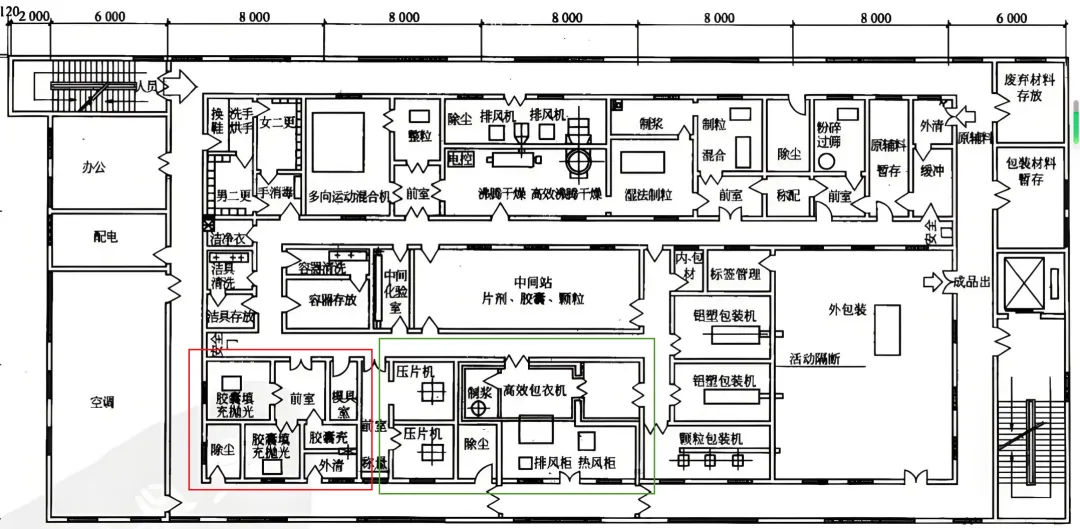
假设一家药品生产企业拥有一条成熟的片剂生产线,现在计划增加胶囊剂产品。由于胶囊剂与片剂生产在同一车间内,在功能间、生产设备上很多存在共用的情形,比如称量、粉碎、制粒、混合等操作间和设备。只是片剂产品有专用的压片间、胶囊剂有专用的胶囊填充和抛光间。我放了一张布局图,从网上找的,大概能展现我假设的情形。现阶段,企业计划向省药监局申报《药品生产许可证》增加生产范围时,企业面临两种申报策略的选择:- 策略二:将原“片剂生产线”更名为“口服固体制剂生产线”,在该生产线项下增加胶囊剂。
类似的情形还有片剂生产线增加颗粒剂产品,注射液生产线增加冻干产品。这两种策略到底有什么不同?哪种更适合企业的长远发展?今天我们就来详细拆解。当然,这里还需要一个假设。假设省药监局对此类情形的生产线命名和管理方式,更多依据企业自行决定。在深入分析之前,需要先明确一个前提:无论选择哪种策略,实际上都是共线生产。因为胶囊剂和片剂共用同一车间的功能间和生产设备,都需要进行共线生产风险评估和清洁验证。这不是“两条独立生产线”的问题,而是“一条生产线上生产两种剂型”的问题。明确了这一点,我们再聚焦文章讨论的核心----行政许可申报路径的选择差异。本文不讨论共线生产的管控。核心差异是GMP符合性检查要求,新增生产线肯定引发GMP符合性检查,但变更生产线(改变功能间用途、增加生产设备)可能不用开展GMP符合性检查。还有,GMP符合性检查是针对生产线开展,未来GMP符合性检查跟踪检查,接受检查频次可能会更少。基于上述对比,从合规效率和长期发展角度,策略二(变更生产线名称+增加生产范围)是更优的选择,主要基于三点考虑:①避免重复建设,符合柔性生产实际。将生产线定义为“口服固体制剂生产线”更符合企业实际的柔性生产模式。片剂、颗粒剂、胶囊剂等口服固体剂型在制粒、干燥、总混等工序上具有高度共通性,一次变更即可覆盖未来可能增加的其他剂型,无需反复申报“新增生产线”。
- ② 行政成本较低,缩短产品上市周期。相比于“新增生产线”必须经历的GMP符合性检查,策略二通常对应的是关键设施变更,往往纳入年度计划检查。这意味着企业可以更快地获得生产资格,加快产品上市步伐。
- ③ 逻辑自洽,避免解释困境。如果设备完全共用,却强行申报为两条独立生产线,在现场检查时反而可能面临“既然设备共用,为何申报为两条线”的疑问,增加不必要的解释成本。
正式申报前,建议携带车间布局图和工艺资料,与当地省药监局进行事前沟通,确认他们对“生产线更名”及“关键设施变化”的认定标准。不同地区的执行尺度可能略有差异,提前沟通可以避免走弯路。这是支撑策略二合规性的核心技术文件。报告应重点包括:产品特性评估(颜色、气味、活性、毒性等)、工艺设备共用情况分析、交叉污染风险识别与控制措施、生产排产与清洁切换流程。必须进行清洁验证,证明切换生产不同产品时,清洁程序能有效防止交叉污染。验证应包括:最难清洁物质的确定、残留限度标准的制定、清洁方法有效性的确认。生产线名称变更,会引发体系文件中文字表述的变更,还可能引发控制策略的变更,需要重新梳理文件体系,避免表述不一致、实际生产控制与文件规定不一致。在药品生产许可证申报中,策略的选择不仅关系到眼前的审批效率,更影响着企业未来的发展空间。当然,无论选择哪种策略,扎实的风险评估和严格的质量管理都是基础。只有在合规的基础上追求效率,才能走得更稳、更远。