
德大医械成立于2014年,专注从事医械产品上市前的法规、技术领域咨询等服务。主营业务:产品注册,临床试验、同品种评价、海外注册、进口注册、质量体系建立及维护、技术转移、医工转化、概念验证等。经过近10年的不断发展壮大,德大建立了一支行业实操经验丰富,充满活力的服务团队,并与国内多家临床机构及检测公司建立了良好的合作关系;德大团队坚持为客户提供一站式管家式服务,旨在帮助客户最大程度降低注册风险、缩短项目周期、 加速产品早日上市。
公司特点:针对不同品种医疗器械提供个性化咨询服务。
德大医械有若干技术讨论群,欢迎医械行业同仁进群,与大家交流技术及工作问题。
在2026植入介入医疗器械创新大会暨第四届心脑血管医疗器械创新发展大会上,德大咨询顾维曼老师就脑机接口(BCI)医疗器械的注册申报与合规策略发表了专题演讲,深入剖析了“植入”与“介入”时代下,BCI技术从研发走向临床的关键路径。
德大医械以参展方身份深度参与大会,与众多合作伙伴及行业同仁共同探讨脑机接口技术临床落地的挑战与机遇。

精准定位,厘清监管路径是首要前提
顾老师在演讲中强调,“合规是基”。BCI产品因其技术路径多样,首要任务是明确监管定位。
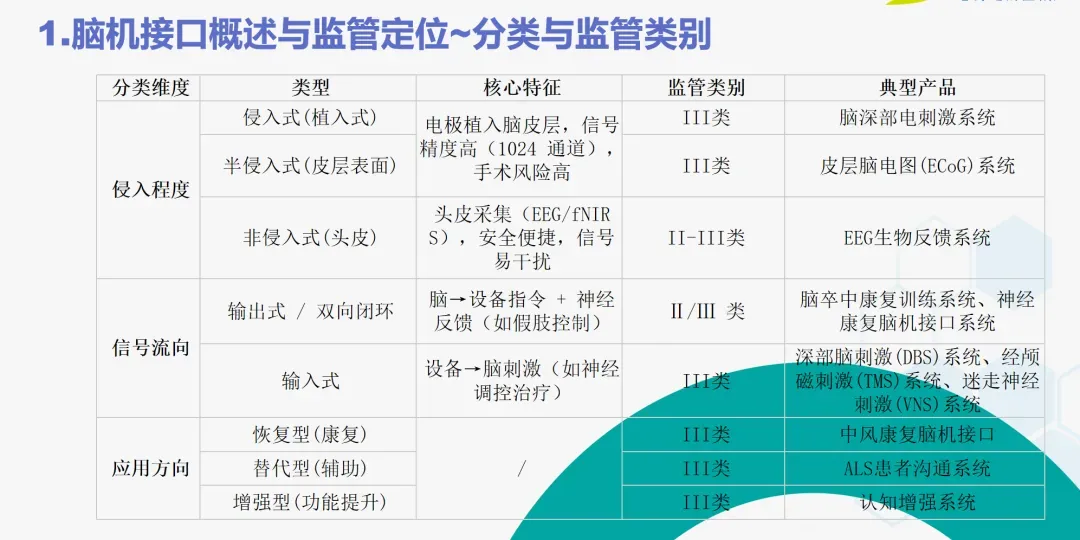
侵入程度决定风险等级:从非侵入式(如EEG头戴设备,通常为II/III类)到半侵入/植入式(如皮层ECoG或深度植入电极,均为III类),监管要求和审评重点截然不同。
功能界定影响分类:即使是“非侵入”设备,若涉及主动的神经调控功能,也可能被界定为更高的管理类别。企业必须在研发初期就与法规团队紧密合作,明确产品分类与所适用的标准体系,避免后期因分类界定不清而推倒重来。

1.脑机接口概述与监管定位
2.法规框架与注册路径
3.技术支持体系与验证要求
4.审评关注核心要点
5.典型案例分享
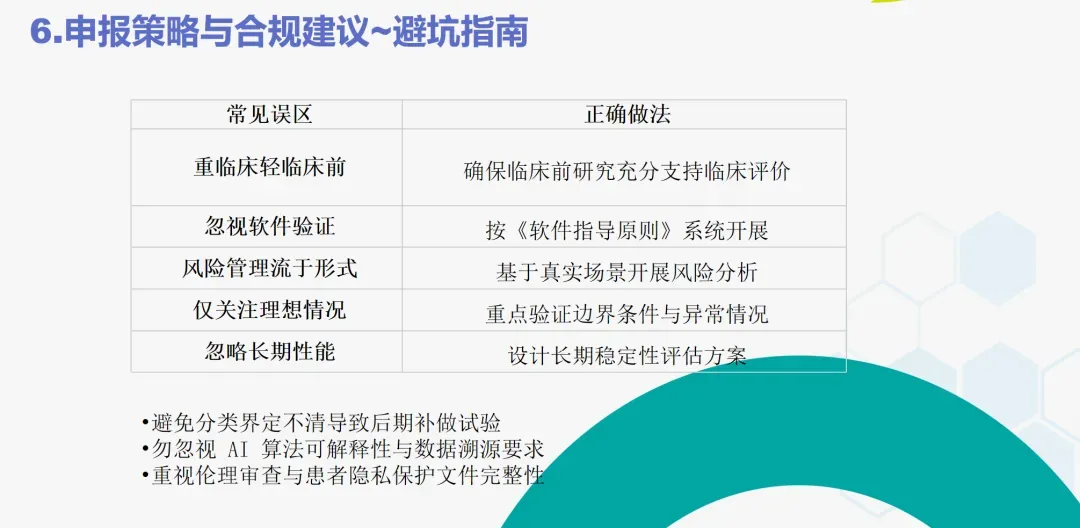
6.申报策略与合规建议



END



