
关注康薪KANGLIFE,获取更多IVD及临床法规最新资讯

康薪咨询
KANGLIFE CONSULTING
美国食品药品监督管理局FDA于当地时间2026年2月17日更新了2025年第四季度GUDID(全球唯一器械识别数据库)报告呈现了在FDA UDI合规执行之后整体情况,本期就将此份报告解读美国FDA UDI 推行现状及2026年医疗器械及IVD器械制造商将如何着手应对。
(*说明:报告数据截至 2025 年 12 月 8 日,所有内容均为 FDA 相关 GUDID(全球唯一器械识别数据库)统计分析)
01
2013-2025年美国GUDID总记录
及提交趋势图
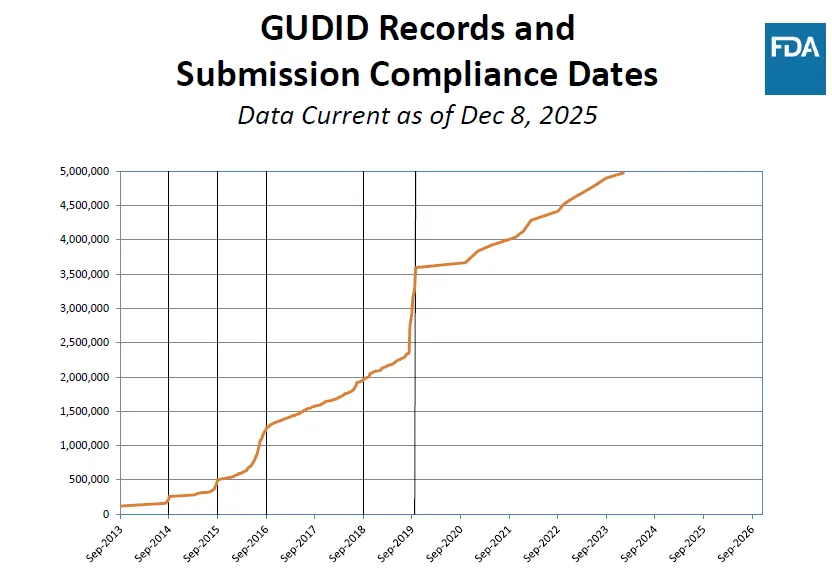
截至 2025 年 12 月8日,GUDID 记录数在 FDA UDI 合规强制要求驱动下持续攀升,快速增长并增长至 500 万条。
从 2013 年 9 月到 2025 年 12 月,GUDID 总记录数从接近 0 条增长至近 500 万条,反映出全球医疗器械企业对美国市场准入及 UDI 合规的持续投入。
曲线呈现明显的阶梯式增长,与 FDA 关键 UDI 合规强制日期高度相关。增长并非自然发生,而是由 FDA 监管政策(尤其是 UDI 强制合规要求)驱动,企业为满足法规要求主动录入产品信息。
随着 2026 年 QMSR 生效、eCTD3.0 深化、DeNovo/510(k) 电子提交及 AI/ML 设备监管框架落地,GUDID 作为核心产品信息数据库的重要性将进一步提升,数据规模与质量要求预计持续升级。
(*图片来源:FDA)
02
GUDID 月度新增企业数走势
UDI 强制节点驱动 GUDID 企业注册出现阶段性爆发,后续维持常态化高基数。
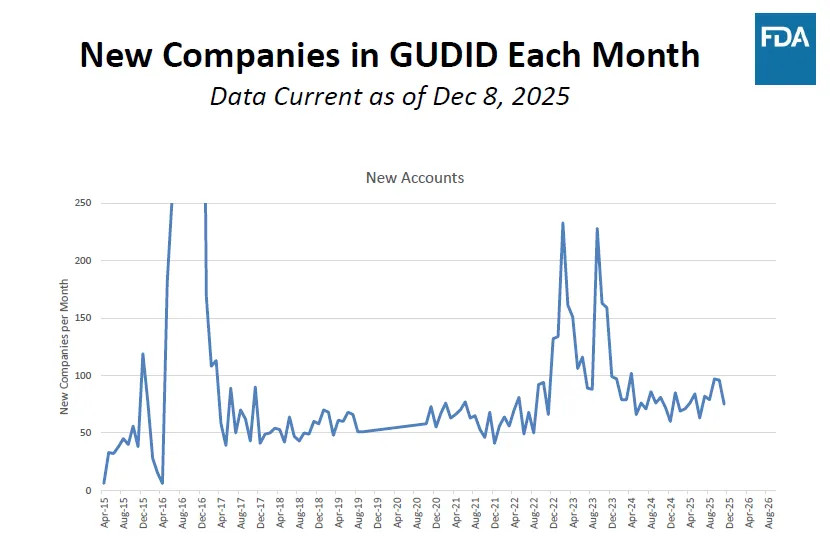
GUDID 月度新增企业数走势图,核心揭示了FDA UDI 合规政策的阶段性强制节点直接驱动企业注册高峰,且全球器械企业对美市场准入的参与度已进入常态化高基数阶段:
合规节点触发注册爆发:图中 2016 年与 2023 年的两次显著峰值,精准对应 FDA UDI 法规的关键强制截止日期。
常态化高基数参与:峰值过后,月度新增企业数并未回落至低位,而是稳定在 50-100 家的区间,反映出美国医疗器械市场的持续吸引力,以及 UDI 合规已成为企业进入美市场的基础门槛,新企业入驻形成常态化趋势。
全球合规意识深化:从 2015 年至今的波动增长轨迹,体现了包括中国在内的全球器械企业,对 FDA 监管规则的响应效率持续提升,合规布局从被动应对转向主动规划。
(*图片来源:FDA)
03
GUDID 数据库中医疗器械的结构特征
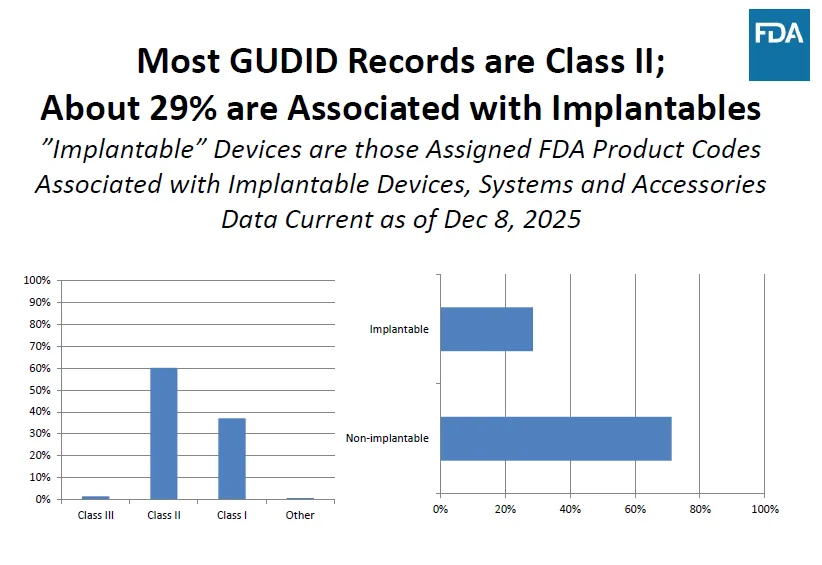
GUDID 记录以 II 类器械为主体,约 29% 为植入式高风险器械,凸显 FDA 监管重点品类特征。
主体为 II 类器械:在 GUDID 记录中,Class II(II 类)器械占比最高,这与美国市场上 II 类器械数量最多、监管强度中等的特点高度一致。
高风险品类占比显著:约29% 的记录与植入式器械(Implantable)相关,这类器械属于高风险品类,是 FDA 重点监管的对象,也意味着相关企业在 2026 年 QMSR、RWE 等新规下将面临更严格的合规要求。
监管重点明确:II 类器械与植入式器械的双重高占比,直接指向 FDA 在 2026 年的监管核心 —— 对高风险、高数量品类的生产质量、上市后监督与数据合规进行强化管理。
(*图片来源:FDA)
04
GUDID 数据库中医疗器械
按医学专科的分布情况
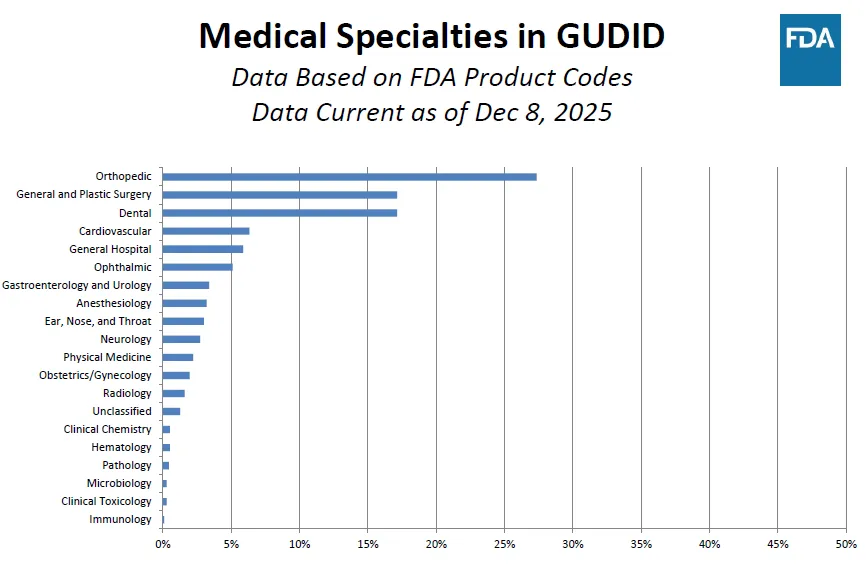
GUDID 中骨科器械占比最高,普通与整形外科、牙科紧随其后,高风险专科成为 FDA 监管核心领域。
骨科(Orthopedic) 是占比最高的专科,在 GUDID 中占据绝对主导地位,反映出骨科器械是美国市场上数量最多、监管最受关注的品类之一。
普通与整形外科(General and Plastic Surgery) 和 牙科(Dental) 紧随其后,构成了 GUDID 中第二梯队的核心专科,这三类专科合计占比超过 40%,是美国医疗器械市场的主流领域。
心血管(Cardiovascular)、综合医院(General Hospital)、眼科(Ophthalmic) 等专科也占据了显著份额,体现出美国医疗器械市场在高风险、高需求领域的布局特点。
从监管视角看,骨科、心血管等植入式器械集中的专科,将是 2026 年 FDA QMSR、RWE 及 UDI 强化监管的核心重点,相关企业需重点关注生产质量、上市后数据与合规更新。
(*图片来源:FDA)
05
GUDID 数据库中频繁出现FDA产品代码术语
GUDID 高频产品代码术语集中于骨科植入与高风险外科器械,材料与智能化特征凸显 FDA 监管与行业创新方向。
骨科与植入式器械是核心:词云中 “Orthopedic(骨科)”、“Implant(植入物)”、“Spinal(脊柱)”、“Hip(髋)”、“Knee(膝)”、“Prosthesis(假体)” 等术语最为突出,这与前序图表中骨科器械占比最高、植入式器械重点关注的结论吻合,印证了骨科植入物是美国医疗器械市场的核心品类。
高风险外科器械密集:“Screw(螺钉)”、“Fusion(融合)”、“Cemented(骨水泥)”、“Electrode(电极)”、“Surgical(外科)” 等术语高频出现,反映出 GUDID 中大量记录为高风险的骨科植入、脊柱手术及心血管介入器械,这些正是 FDA 2026 年 QMSR、RWE 及上市后监督的重点监管对象。
材料与技术特征显著:“Polymer/Metal/Polymer(聚合物 / 金属 / 聚合物)”、“Porcelain(瓷)”、“Resin(树脂)”、“Synthetic(合成材料)” 等材料术语,以及 “AI(人工智能)”、“Wireless(无线)”、“Photosensitive(光敏)” 等技术术语,体现出当前器械在材料创新与智能化方面的发展趋势,也意味着企业在合规中需重点关注材料生物相容性与 AI 算法监管。
合规提示明确:高频术语直接指向了 FDA 产品代码的核心分类,企业在录入 GUDID 或进行 510 (k)/PMA 申请时,需确保产品代码术语与 FDA 官方标准完全一致,避免因术语不标准导致等价器械识别失败或审评延误。
06
GUDID 标签商的全球地域分布
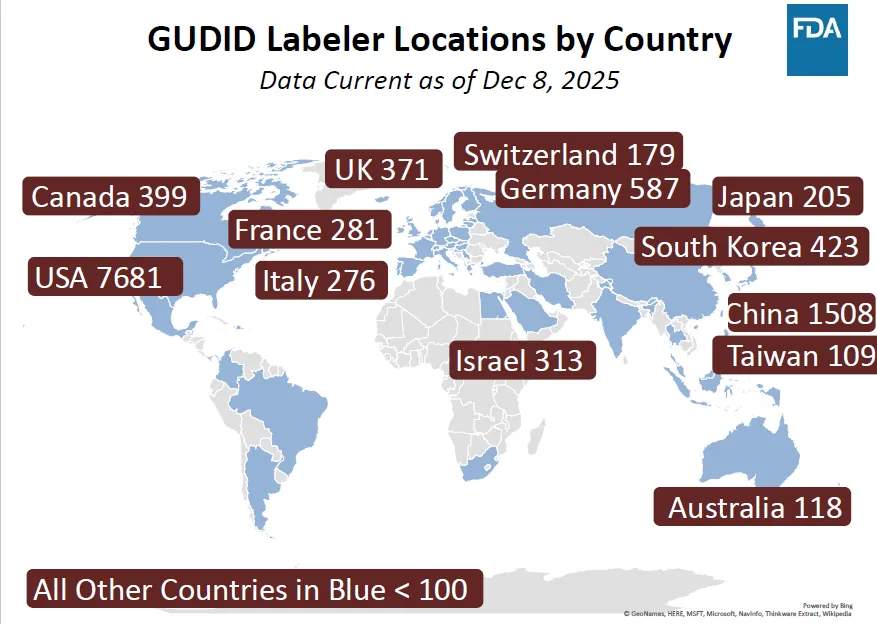
GUDID 标签商以美国为核心,中国为最大境外来源,形成中美主导、欧亚多国参与的全球产业格局
美国本土标签商占据绝对主导:美国以 7681 家标签商数量遥遥领先,这反映出美国本土医疗器械产业的规模和成熟度,同时也说明美国企业是 FDA 监管体系的核心。
中国是最大的境外标签商来源地:中国以 1508 家标签商位列第二,远超德国、韩国等其他国家,这体现了中国医疗器械企业对美国市场的高度重视和深度参与,也意味着中国企业将是 2026 年 FDA 新规(如供应链溯源、UDI 强化)的重点影响群体。
欧洲与亚洲是重要的境外市场:德国(587 家)、韩国(423 家)、英国(371 家)、以色列(313 家)等国家和地区的标签商数量也位居前列,形成了以中美为核心、欧亚多国参与的全球产业格局。
合规挑战呈现地域差异化:
美国本土企业需率先完成 QMSR 等新规的体系升级;
中国、德国等境外标签商则需重点应对供应链溯源、境外生产厂核查等进口器械专项要求;
所有企业都需确保 GUDID 数据与 eCTD 等系统的实时同步,以满足 2026 年跨系统数据校验的合规要求。
(*图片来源:FDA)
2026 年 GUDID 展望与监管趋势
| 核心监管新规驱动
QMSR 生效:2026 年 2 月起,质量管理体系法规(QMSR)取代旧版 QSR 820,对植入式等高风险器械提出生产过程验证、CPK 数据、供应链质量协议等更严苛要求。
UDI 与上市后监督强化:UDI 将与召回、MDR(不良事件报告)深度联动,植入式器械 UDI 信息的准确性、产品核心信息 / 不良事件相关重大变更的及时性成为审核重点。
电子化递交深化:GUDID 数据需与电子化提交的技术文件自动匹配,不一致将直接触发审评暂停,跨系统数据校验成为硬性门槛。
AI/ML 设备监管框架落地:AI 赋能器械(如骨科导航、心脏影像设备)需提交算法生命周期档案,并在 GUDID 中明确标注 AI 属性。
| 企业合规重点
美国本土企业:优先完成 QMSR 与现有体系的差距分析,搭建 RWE 数据采集体系,确保 GUDID 与生产、质量数据实时同步。
中国等境外企业:重点应对供应链溯源合规,完成核心元器件供应商资质备案、供应链流程图可视化及境外生产厂 FDA 核查记录提交。
高风险品类企业:植入式、II 类器械企业需重点满足 QMSR 生产端要求与 RWE 强制纳入,确保 UDI 变更响应及时。
| GUDID 角色升级
GUDID 将从单纯的产品信息录入库,升级为QMSR、eCTD3.0、UDI 监管、RWE 应用的核心衔接点,其数据的标准化、及时性、联动性将直接决定企业 510 (k)/PMA 申请的成败。
给医疗器械制造商和IVD制造商的建议
体系升级:尽早完成QMSR差距分析,补充植入式器械CPK数据、过程验证报告,并按FDA标准梳理GUDID分类信息;IIb类及以上植入设备搭建OMOP标准RWE框架。
GUDID管理:建立GUDID-电子递交联动机制,IVD重点校验试剂批号等参数一致性。
供应链合规:植入式器械提交CPK数据;准备供应链流程图,备案核心供应商资质及FDA核查记录,并制定中断应对方案。
专项合规:含AI器械标注AI属性并提交算法档案;IVD建立性能监测体系持续更新数据;高风险器械强化UDI与MDR关联分析,及时同步风险信息。
康薪咨询全球化合规一站式服务
康薪咨询自成立以来,致力于为医疗器械及IVD企业提供全生命周期合规服务,助力本土企业高效突破国际法规壁垒、实现全球化布局:
临床试验服务:依托欧洲、泰国等地战略合作实验室与医院,提供临床前性能验证、临床试验、上市后评估等全链条临床服务
国际法规注册:覆盖欧盟IVDR/MDR、中国NMPA、美国FDA、英国MHRA、澳大利亚TGA、日本PMDA、韩国MFDS、新加坡HSA、泰国TFDA、马来西亚MDA、沙特SFDA、阿联酋MOHAP、巴西ANVISA、墨西哥COFEPRIS等全球主要市场的技术文件辅导与申报;
质量管理体系:ISO 13485、MDSAP等国际质量体系搭建与认证支持;
出海战略支持:当地授权代表服务、出海战略规划及合规人才培养等
*资料来源:FDA《FDA GUDID 2025》
*声明:本文章报告内容均为转载,仅用于分享,如涉及版权等问题,请随时与我们取得联系,我们将于第一时间进行修正,谢谢。
康薪咨询团队可承接欧洲多国、泰国、中国等多国医疗器械及IVD器械注册要求的临床实验研究项目(可出具伦理批件),可为IVD企业提供全生命周期的解决方案服务。
康薪KANGLIFE
业务范围
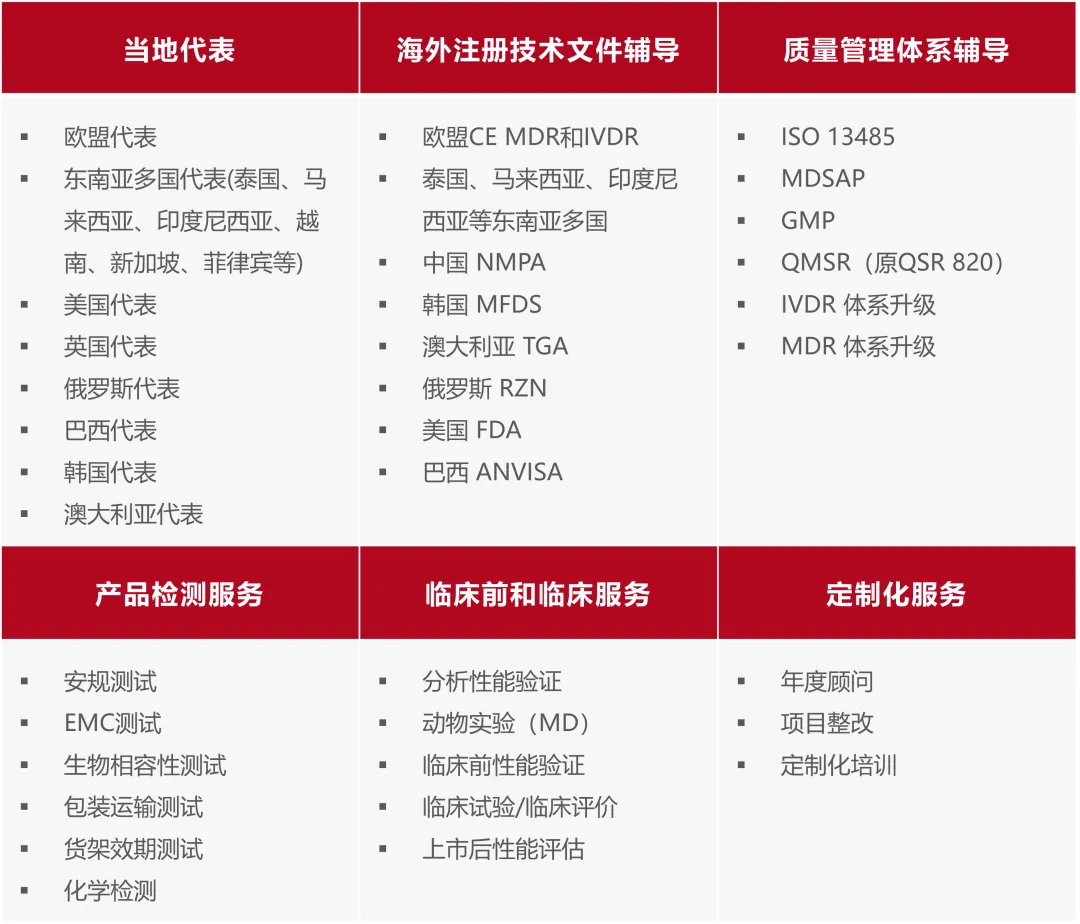
注册服务支持区域
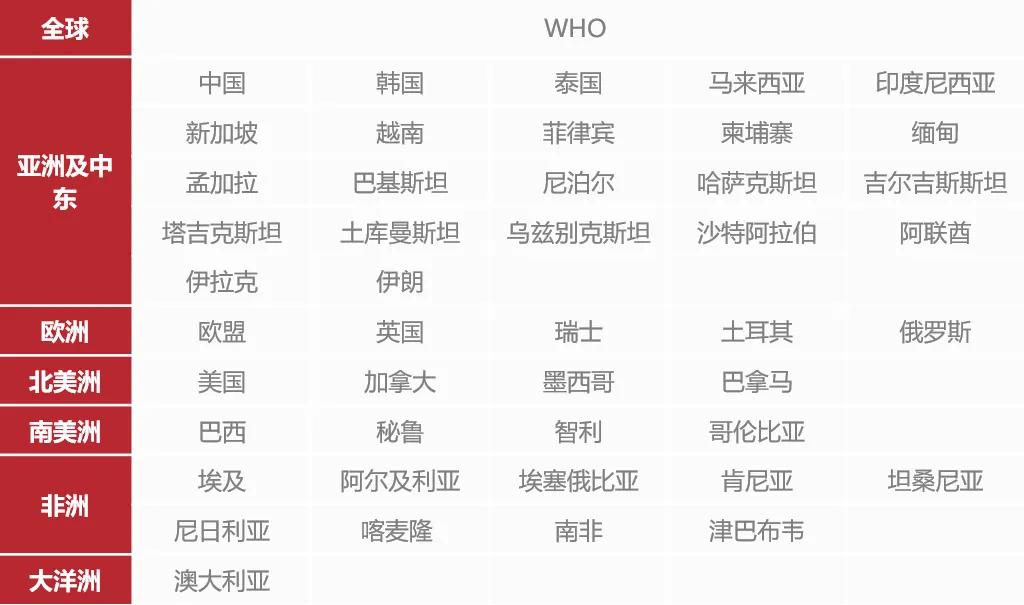
临床实验室资源

关于康薪咨询
ABOUT KANGLIFE
| 专业特色:
协同企业,共同定制出海战略服务。
| 核心文化:
协助国内外优秀体外诊断及医疗器械企业实现战略发展、培养合规人才,携手共筑中国企业出海愿景。
康薪咨询成立以来已与数百家企业强强联合,协同高效合作,提供定制化服务,成功获得多个欧美和东南亚市场准入资质。
推荐阅读
业务咨询
CONTACT US

华北区咨询顾问
Harold Hua

华东区咨询顾问
Joyce Hua

华南区咨询顾问
Fitter Cao


关注康薪咨询
Follow KANGLIFE
点击下方”阅读原文“,即刻与我们取得进一步联系!

